精读分享│【Nature Cancer】:转录和DNA复制碰撞导致大量串联重复并暴露癌症靶向治疗的脆弱性
英文题目:Transcription and DNA replication collisions lead to large tandem duplications and expose targetable therapeutic vulnerabilities in cancer 中文题目:转录和DNA复制碰撞导致大量串联重复并暴露癌症靶向治疗的脆弱性 期刊:Nature Cancer(IF: 23.5) 单位:芝加哥大学人体遗传学系 发表时间:2024年11月
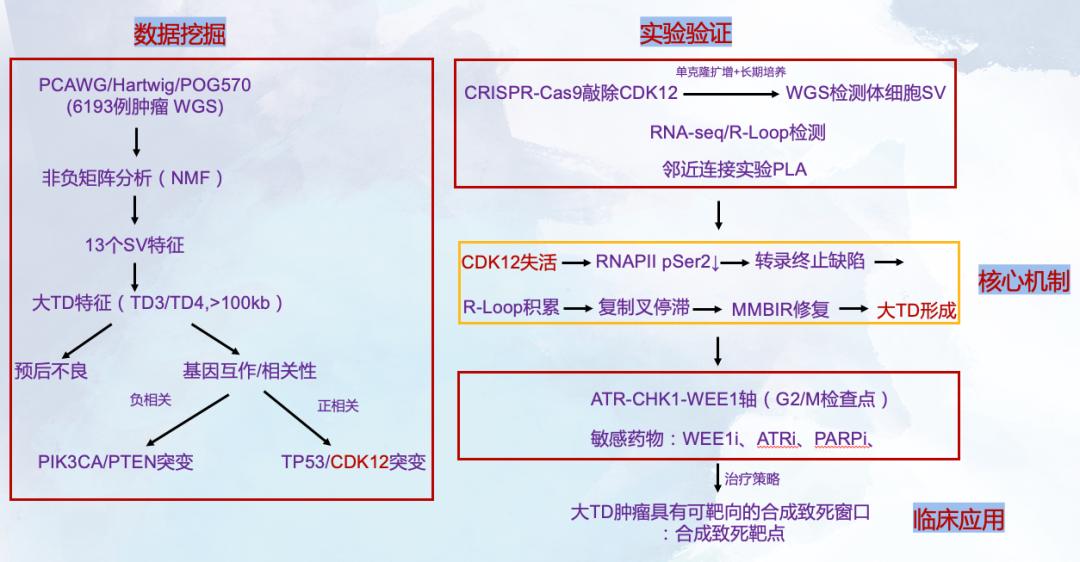
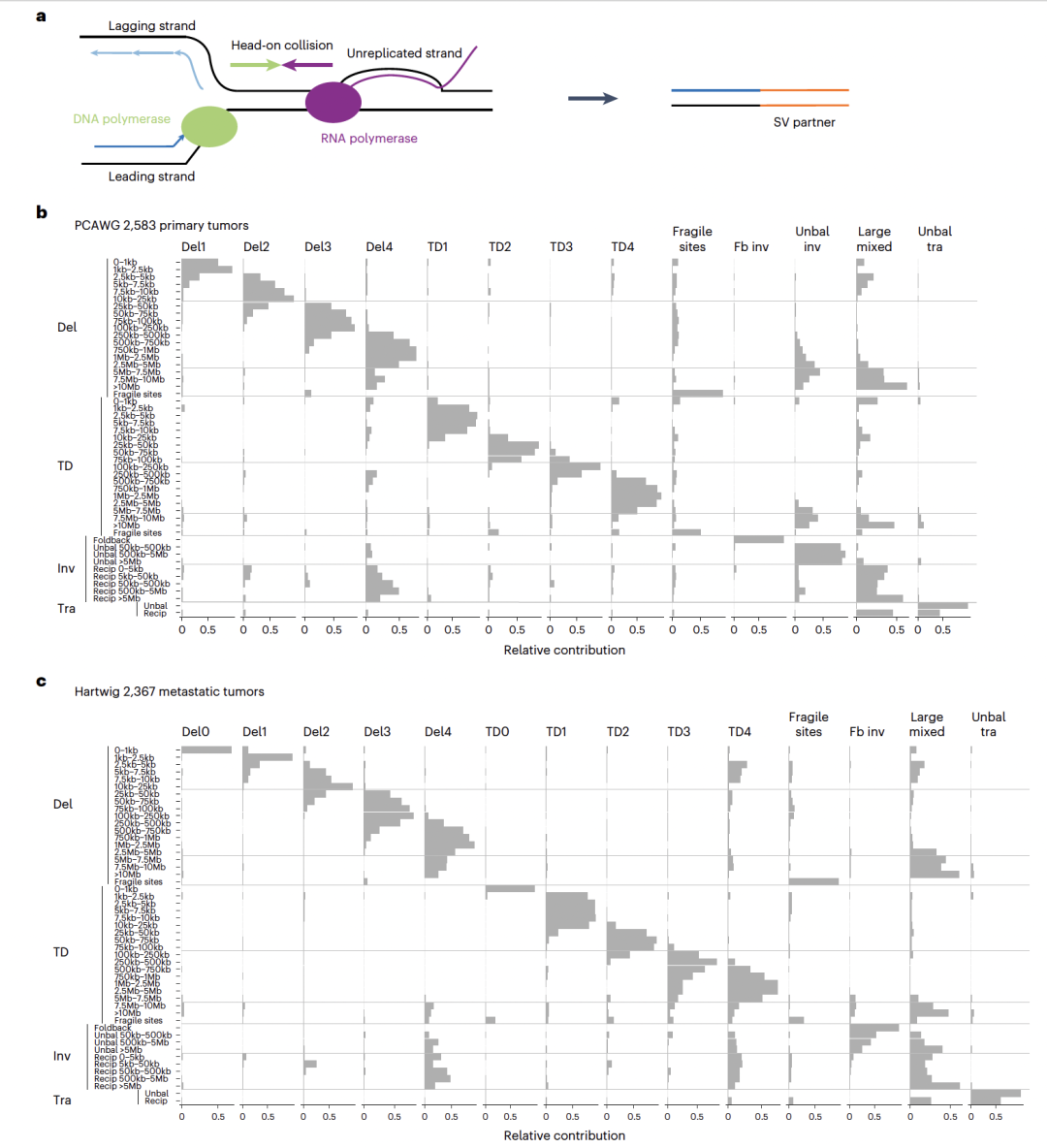
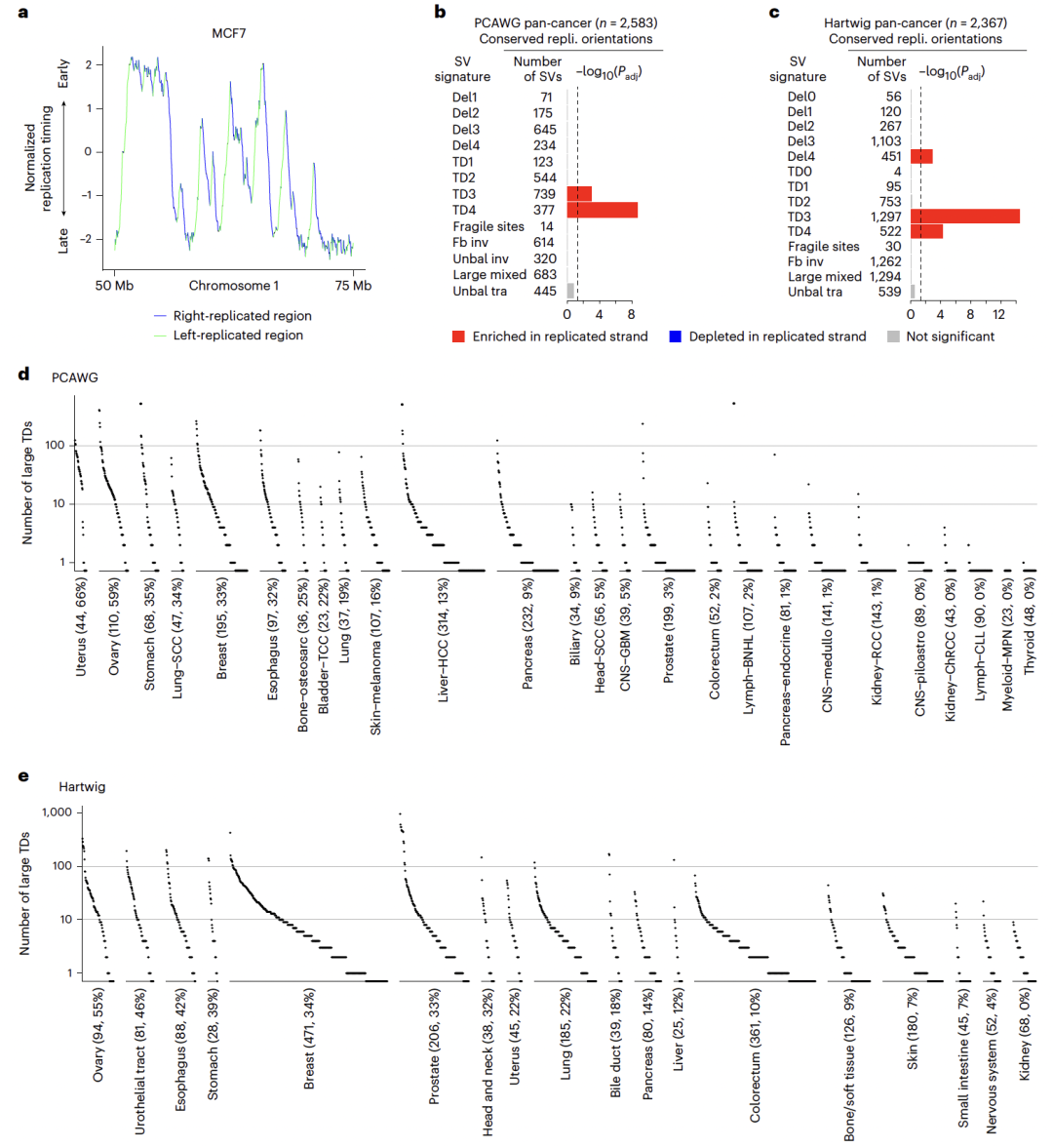
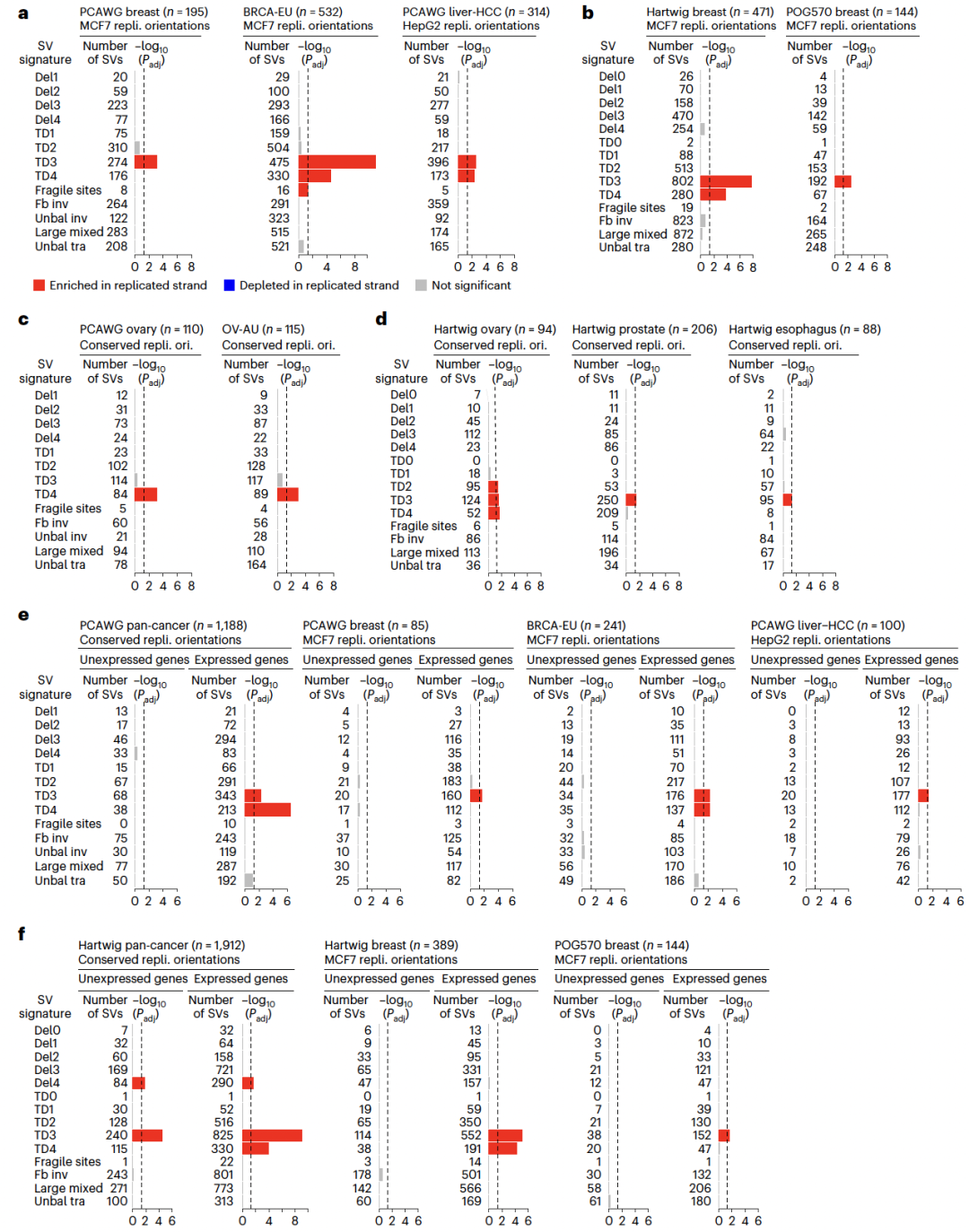
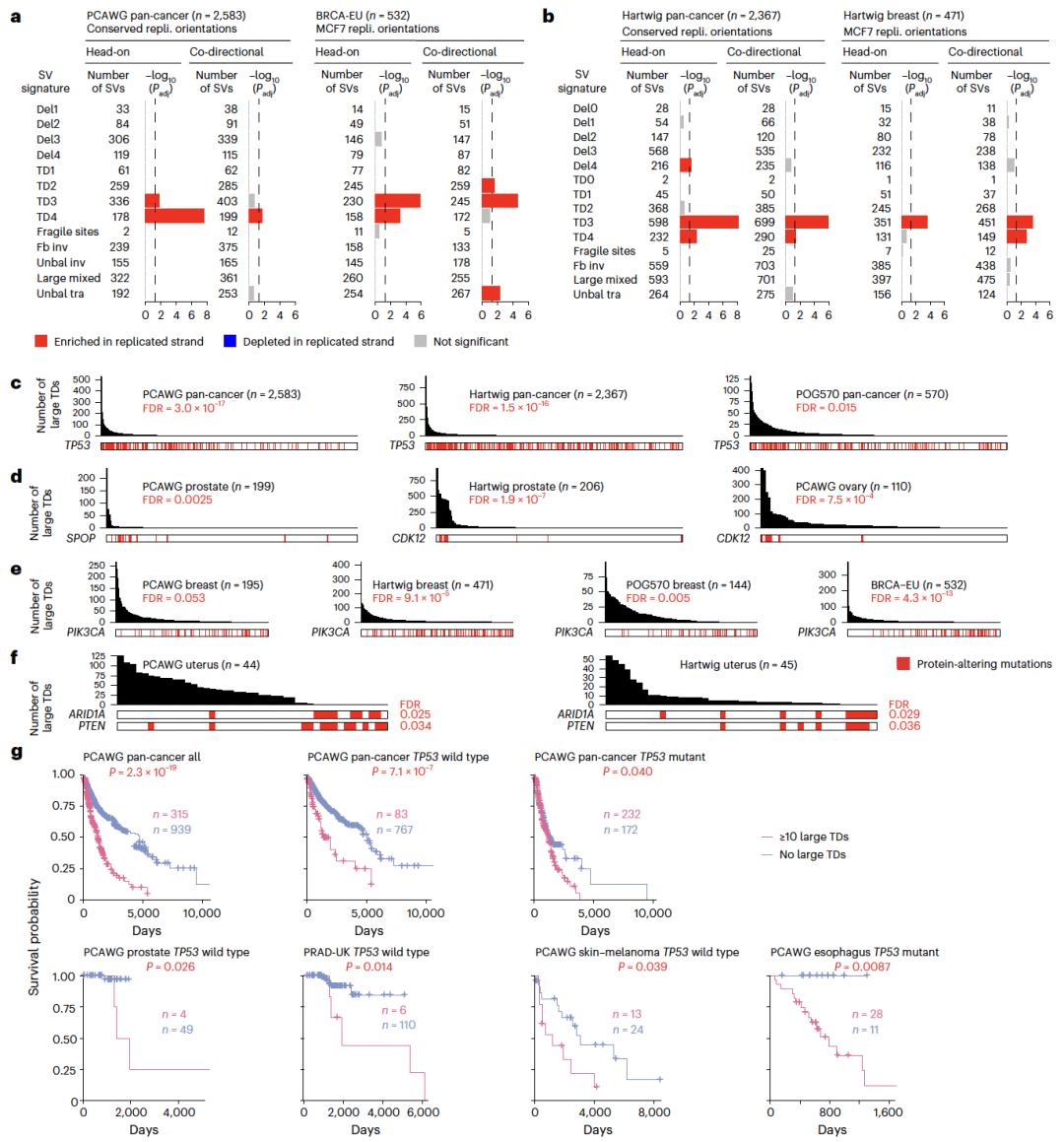
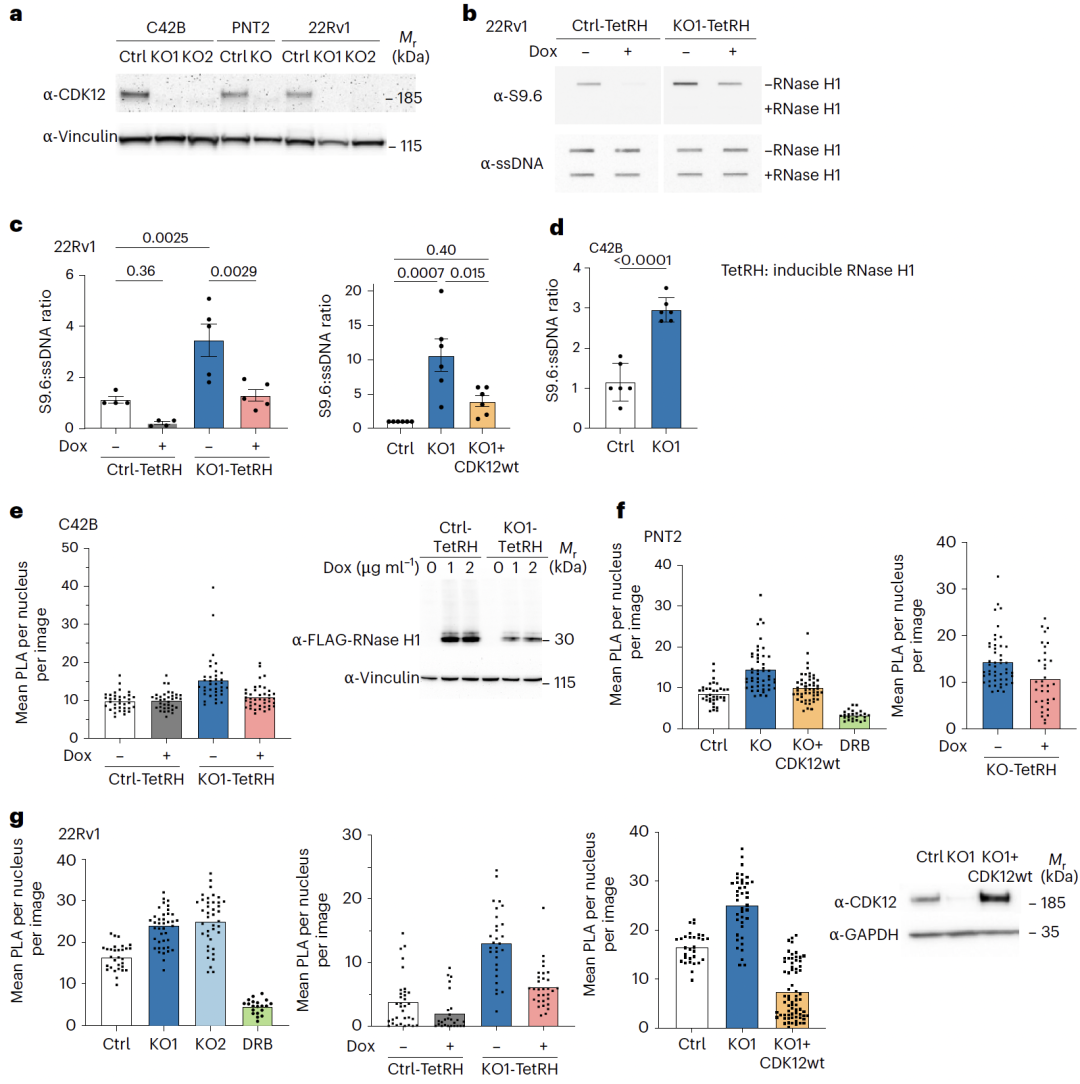
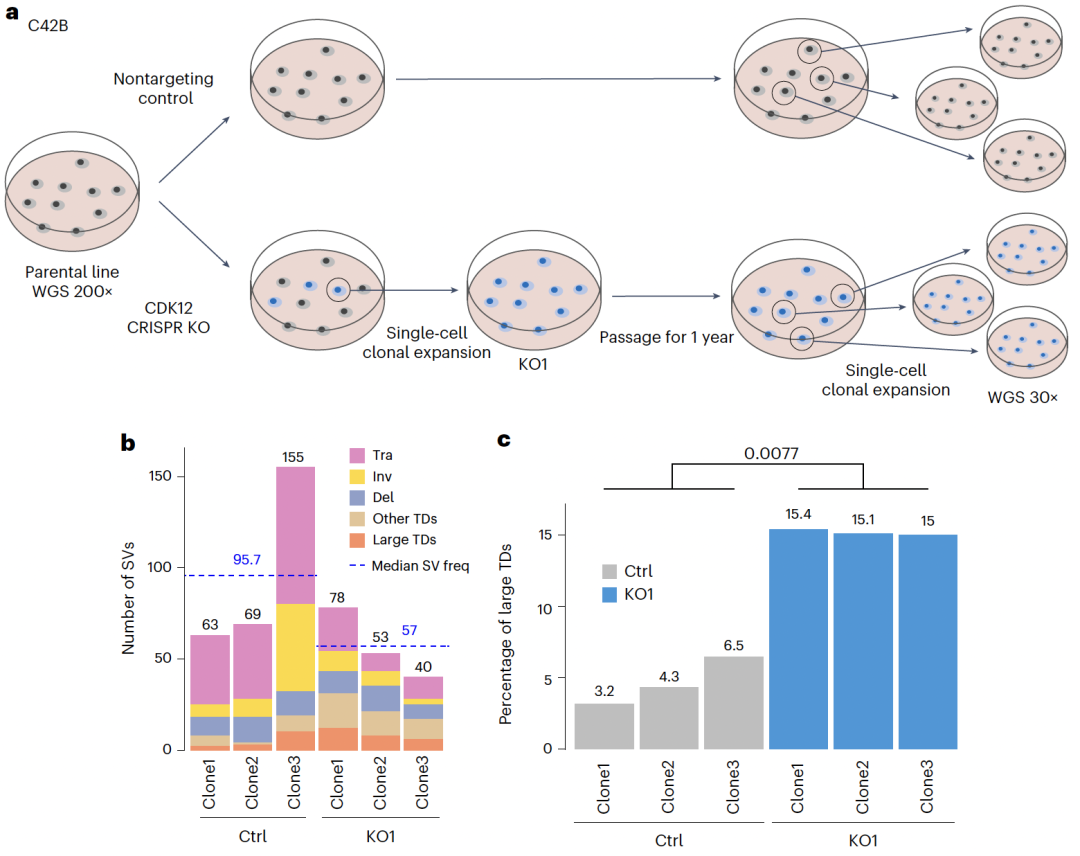
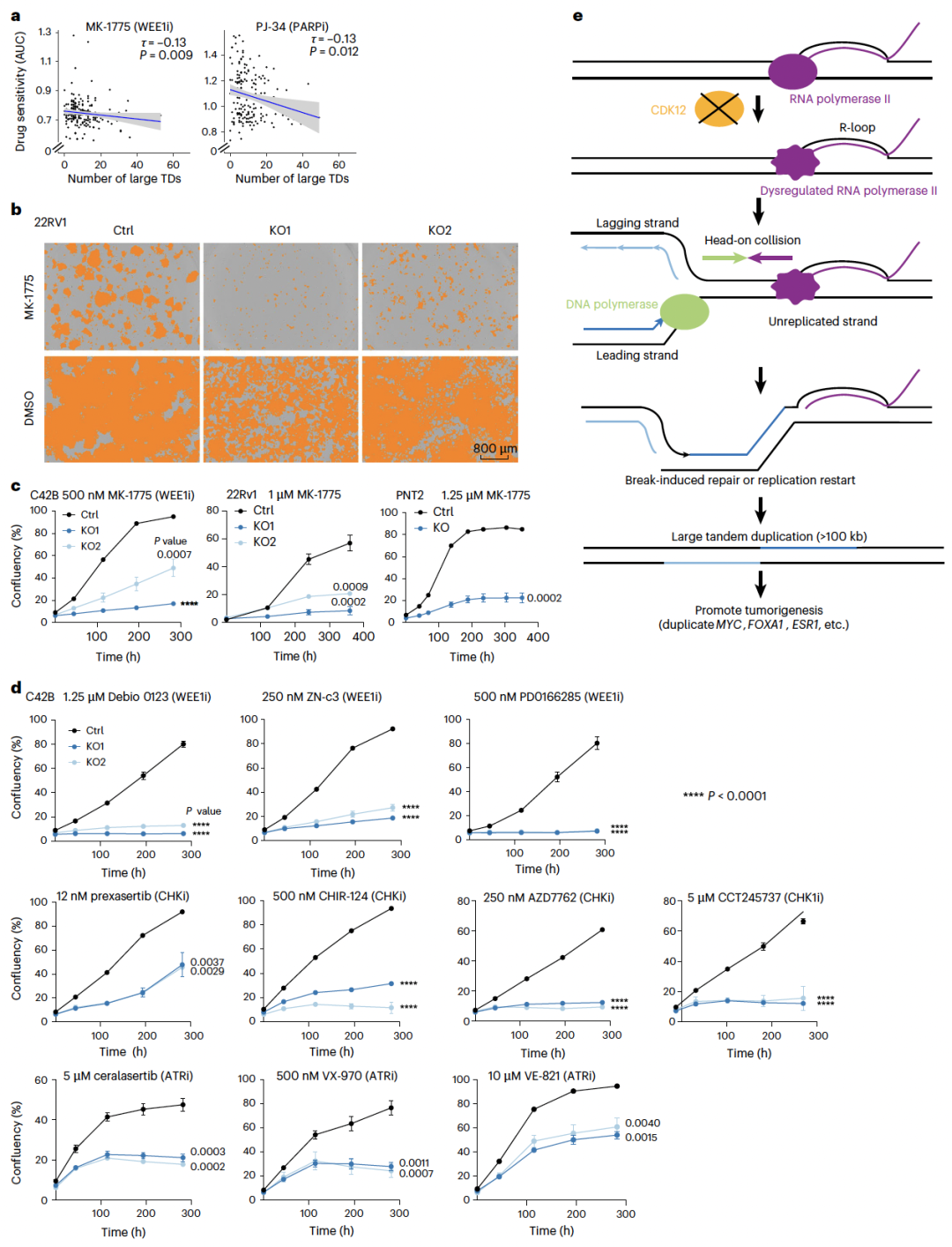
摘要: 尽管癌症中体细胞结构变异(structural variations,SVs)明显富集,但其形成的分子机制仍不清楚。本研究基于6,193例全基因组测序肿瘤样本,系统分析了转录与DNA复制冲突对基因组不稳定性的影响。在对三个相互独立的泛癌队列中的稳健SV特征进行反卷积分析后,研究者在大型串联重复(large tandem duplications,TDs)中检测到转录依赖性的复制链偏向性,这正是转录–复制冲突(transcription–replication collision,TRC)的典型分子足迹。大型TDs在女性患者中更为常见的上消化道肿瘤和前列腺癌中尤为丰富,并与患者不良生存结局以及TP53、CDK12和SPOP基因突变显著相关。CDK12失活后,细胞中TRC事件、R环以及大型TDs的数量均显著增加。此外,抑制 WEE1、CHK1 或 ATR 可选择性地抑制 CDK12 缺失细胞的生长。综上所述,该研究表明,癌症中的大型TDs源于转录–复制冲突,其存在可作为预后评估和治疗决策的生物标志物。 思维导图: 研究背景: 基因组不稳定性是癌症的典型特征之一,其中结构变异(structural variations,SVs)在多种人类癌症,尤其是实体瘤中广泛存在。然而,除少数情形外,SV形成的分子机制仍知之甚少。已有研究表明,在乳腺癌、卵巢癌、前列腺癌和胰腺癌中,BRCA1/2突变导致的同源重组修复缺陷可解释部分小缺失和小型串联重复,而在淋巴系统肿瘤中,异常的V(D)J重排可引发染色体易位,但这些机制无法覆盖大多数肿瘤类型中普遍存在的大量体细胞SV。阐明SV形成的分子基础具有重要的临床意义,不仅有助于肿瘤风险评估和早期筛查,也为发现可靶向的治疗通路提供依据。DNA复制压力被认为是基因组不稳定性的主要来源之一,而转录与DNA复制在同一模板上的不可避免碰撞(transcription–replication collision,TRC)可能通过R环积累、复制叉崩溃及DNA断裂,促进基因组结构异常的产生。尽管TRC已被证明在多种模型体系中可诱发突变和染色体损伤,其在人类癌症中驱动SV形成的作用仍不明确。基于此,本研究对6,193例全基因组测序肿瘤进行了系统分析,旨在揭示TRC在体细胞结构变异形成中的作用,并探索其潜在的临床治疗价值。 主要结果: 1、人类癌症中的简单SV特征 Fig 1. TRC and simple SV signatures 基于非负矩阵分解(non-negative matrix factorization,NMF)的突变特征分解方法在提取突变特征并推断体细胞单核苷酸变异(single-nucleotide variants,SNVs)、拷贝数变异(copy number variations,CNVs)、结构变异(SVs)以及染色体不稳定性背后的分子机制方面表现出极高的有效性。在全基因组泛癌分析(Pan-Cancer Analysis of Whole Genomes,PCAWG)队列中鉴定出六种复杂SV特征,并发现其中一种与环状染色体外DNA相关,且在转录–复制冲突(transcription–replication collision,TRC)区域表现出明显偏倚。本研究则进一步聚焦于简单SV(包括缺失、重复、倒位和易位)中的TRC相关特征。 研究假设,癌症中一部分体细胞简单SV来源于转录–复制冲突未被正确修复的结果。鉴于基于NMF的特征分析能够稳健地捕捉潜在分子机制,研究人员选用了三个大规模、泛癌的全基因组测序(WGS)队列,对简单SV特征进行系统推断:PCAWG队列(涵盖39种肿瘤类型的2,583例原发肿瘤)、Hartwig队列(涵盖36种肿瘤类型的2,367例转移性肿瘤)以及POG570队列(涵盖26种肿瘤类型的570例转移性肿瘤)。三大队列合计共包含5,520例肿瘤样本,使该研究成为目前规模最大的泛癌SV特征分析研究之一。 在这三个队列中,共检测到1,025,587个体细胞SV,其中PCAWG、Hartwig和POG570队列分别包含288,417、668,492和68,678个SV。此前PCAWG研究共鉴定出12种SV特征,但其中既包含简单SV,也包含多种复杂SV(如染色体粉碎、染色体拼接、模板插入循环及模板插入链等)。鉴于前期已证明复杂SV由不同于简单SV的机制形成,因此该研究中排除了所有类型的复杂SV,以更准确地解析简单SV特征。经过筛选,PCAWG、Hartwig和POG570队列中分别保留了133,718、303,905和41,014个简单SV。 为更精细地解析SV大小的影响,研究人员将缺失和串联重复(tandem duplications,TDs)分别划分为18个不同的大小区间。基于SV类型和大小,共将所有简单SV分成49个类别,并采用SigProfilerExtractor进行SV特征分解。在PCAWG队列中共识别出13种SV特征,包括4种缺失特征(Del1–Del4)和4种TD特征(TD1–TD4),以及脆性位点相关SV、折返倒位、不平衡倒位、大型混合SV(包括大型缺失、大型TD、成对倒位和相互易位)和不平衡易位。这13种SV特征与先前报道的12种PCAWG SV特征高度一致,表明NMF方法具有良好的稳健性。缺失和TD特征之间的主要差异主要来源于SV大小分级方式的不同,以及是否在特征分解中引入复制时序信息。此前另有研究提出三种TD表型,分别与该研究中的TD1、TD3和TD4相对应。 在Hartwig队列中,共鉴定出14种SV特征,与PCAWG队列中的特征高度相似,其中新增的两种特征为极小缺失(Del0)和极小TD(TD0),主要源于SV检测算法的差异。POG570队列中获得的SV特征亦与PCAWG和Hartwig队列保持一致。在后续分析中,研究人员将来自其他原发肿瘤队列的简单SV映射至PCAWG鉴定的13种SV特征,并将转移性肿瘤中的简单SV映射至Hartwig队列鉴定的14种SV特征。 2、TRC区域中的SV链偏向性 Fig 2. Pan-cancer replicated-strand bias and large TD frequencies across tumor types 研究为进一步识别由TRCs修复不当所产生的结构变异(SVs)。结果发现,小缺失、脆性位点相关SV以及折返倒位主要富集于晚复制区域,而串联重复(TDs)和不平衡易位则主要富集于早复制区域(Extended Data Fig 2d)。此外,一部分SV在转录活跃的基因中显著富集(Extended Data Fig 3a,b)。然而,究竟哪些SV是由TRC直接导致的,仍有待明确。 在正常细胞中,转录与复制之间的冲突通常可通过多种DNA损伤应答通路(如Fanconi贫血通路)得到有效解决;若修复失败,复制叉坍塌最终可能产生SV(图1a)。关键在于,这类由TRC引发的SV应当携带特异性的遗传学印记。首先,其断点应主要位于基因内部。其次,在TRC发生并导致复制叉坍塌后,断裂位点的一侧DNA已完成复制,而另一侧尚未复制。由于已复制链具有两份拷贝,而未复制链仅有一份拷贝,其中一条已复制链(前导链或后随链之一)更可能与其他DNA片段发生连接,从而形成SV(图1a右)。因此,在SV连接位点处应观察到已复制链的富集,由此产生链偏倚(strand bias);而具体形成哪一类SV,则取决于所选择的修复伴侣。 对于每一个SV断点,都会有两个DNA片段彼此连接,每个片段具有特定的方向性,通常用“+”或“-”表示该片段是以DNA的上游端还是下游端参与连接(Extended Data Fig 3c)。为检测SV的链偏倚,首先利用来源于14种实体组织细胞系的Repli-seq数据,为所有蛋白编码基因定义了保守的复制方向(图2a和Extended Data Fig 3d)。随后,对肿瘤中观测到的所有SV进行随机打乱,并在PCAWG和Hartwig队列中分析至少有一个断点位于蛋白编码基因内的简单SV是否存在链偏倚。通过将真实SV与随机化SV进行比较,结果发现,在两个队列中,TD3和TD4的断点均一致性地富集于已复制链上(图2b,c)。 进一步分析显示,大型TD(TD3和TD4)在子宫癌、卵巢癌和乳腺癌、上消化道肿瘤(食管癌和胃癌)、以及前列腺癌和尿路上皮癌中高度富集(图2d,e)。此外,大型TD在转移性头颈部肿瘤中也较为常见,这些肿瘤同样涉及上消化道相关组织(图2e)。利用乳腺癌细胞系MCF7和肝癌细胞系HepG2中确定的复制方向信息,在四个相互独立的乳腺癌队列(PCAWG、Hartwig、POG570和BRCA-EU)以及肝癌中,均观察到TD3和TD4显著的链偏倚(图3a,b)。类似的链偏倚现象也出现在三个独立的卵巢癌队列(PCAWG、Hartwig和OV-AU)以及转移性前列腺癌和食管癌中(图3c,d)。 如果大型TD确实来源于TRC,那么其链偏倚应当依赖于基因转录水平。与这一假设一致,在PCAWG和Hartwig队列中,在未表达基因中并未观察到TD3或TD4的链偏倚,而在表达基因中则可清晰检测到该偏倚(图3e,f)。使用组织特异性的复制方向信息,在四个独立的乳腺癌队列(PCAWG、Hartwig、POG570和BRCA-EU)及肝癌中,也观察到相同的表达依赖性趋势(图3e,f)。这一表达依赖性的链偏倚同样存在于两个独立的卵巢癌队列中(Extended Data Fig 4a)。考虑到基因表达也可能是SV产生的结果而非原因,进一步采用正常组织的基因表达数据进行分析,结果仍然在TD3和TD4中观察到转录依赖的已复制链偏倚(扩展数据图4b,c)。 综上所述,研究人员在多个相互独立的癌症队列中一致地观察到大型串联重复具有显著的、转录依赖的已复制链偏倚,为其来源于转录–复制冲突提供了有力证据。 Fig 3. Tumor type-specific and transcription-dependent, replicate strand bias 3、在大TDs中,复制链偏向性可作为一种独立效应 Fig 4. Replicated-strand bias in head-on and co-directional collision regions and genetic and clinical associations of large TDs. 接下来,研究人员评估了DNA复制在大TDs链偏倚形成中的作用。TRC主要包括两种形式:正向冲突(head-on),即转录与复制沿相反方向进行;以及同向冲突(co-directional),即二者沿相同方向进行(图1a)。如果大型TD确由TRC产生,那么无论冲突类型如何,均应观察到已复制链偏倚。与这一假设一致,在PCAWG和Hartwig队列中,TD3和TD4在正向冲突和同向冲突条件下均表现出显著的已复制链偏倚(图4a,b)。在BRCA-EU和Hartwig乳腺癌队列中,采用MCF7细胞系注释的复制方向后,也观察到相同结果(图4a,b)。这些结果表明,大型TD中的链偏倚依赖于DNA复制过程本身,而与转录–复制冲突的方向(正向或同向)无关。 鉴于基因组中多种特征(如GC含量、转录活性、复制时序及染色质状态)之间高度相关,进一步排除了大型TD中已复制链偏倚由其他因素驱动的可能性。为此,研究人员构建了多变量回归模型,以SV所连接的链类型(已复制链或未复制链)作为因变量,以真实SV与随机化SV以及一系列基因组特征作为自变量进行分析。在PCAWG队列中,即便在控制其他基因组特征后,真实SV与已复制链的显著相关性仍仅出现在TD3和TD4中(扩展数据图5a)。在Hartwig队列(Extended Data Fig 5b)以及基于MCF7复制时序、合并分析的四个乳腺癌队列中(Extended Data Fig 5c),也观察到相同的显著关联。因此,大型TD中的已复制链偏倚是一种独立效应,不能用其他已知基因组特征加以解释。 随后,进一步探索了参与TRC及大型TD形成的关键基因。系统分析了所有蛋白编码基因中会改变编码序列的体细胞单核苷酸变(Supplementary Table 2)。如预期所示,TP53突变与大型TD显著正相关(图4c),这可能源于TP53缺失使细胞能够耐受更高水平的基因组不稳定性。在前列腺癌中,SPOP突变同样与大型TD显著相关(图4d)。结合研究者此前发现SPOP突变与复杂SV相关的结果,提示突变型SPOP可能与突变型TP53类似,发挥“基因组稳定性守门人”的作用。此外,正如此前报道的那样,CDK12突变(而非BRCA1或BRCA2突变)与卵巢癌和转移性前列腺癌中的大型TD显著相关(图4d及Supplementary Table 2)。BRCA1突变仅与小型TD相关,而不与大型TD相关。基于这一结果,后面的研究中对CDK12进行了更深入的研究。值得注意的是,在四个独立的乳腺癌队列中,发现PIK3CA突变与大型TD呈显著负相关(图4e);同时,ARID1A和PTEN突变在原发及转移性子宫癌中均与大型TD呈负相关(图4f)。 如前所述,大型TD常导致基因的重复扩增。除先前报道的MYC、MALAT1、MECOM、ESR1、ERBB2、FOXA1和MDM2等基因外,还发现GATA3在转移性乳腺癌中频繁扩增,而ERBB3和H3F3B在子宫癌中也常发生扩增(Extended Data Fig 6)。 最后,研究评估了大型TD在临床预后中的潜在价值。在PCAWG队列中,将所有肿瘤类型合并分析后,大型TD高度富集的肿瘤与较差的总体生存期显著相关;即便按TP53突变状态对患者进行分层分析,这一关联仍然存在(图4g)。此外,在两个前列腺癌队列(PCAWG和PRAD-UK)中,以及黑色素瘤和食管癌患者中,大型TD的高丰度同样与不良生存结局显著相关(图4g)。 4、CDK12的缺失可以导致R环和TRCs的累积 Fig 5. Loss of CDK12 results in increased R-loops and TRCs 研究前期已证明CDK12突变与癌症中的大型TDs显著相关,且大型TD呈现出TRC的分子足迹。基于此,提出假设: CDK12失活会导致TRC水平升高。为验证该假设,利用CRISPR–Cas9技术,在两种前列腺癌细胞系(C42B和22Rv1)以及一株永生化正常前列腺上皮细胞系(PNT2)中,构建了来源于单细胞的CDK12敲除(knockout,KO)克隆,共获得5个CDK12 KO克隆(C42B中2个、22Rv1中2个、PNT2中1个;图5a)。通过RNA测序(RNA-seq)验证,这些克隆中均存在双等位基因移码型插入/缺失突变(indels)(Extended Data Fig 7a),且其改变模式与前列腺癌中观察到的CDK12突变高度一致(Extended Data Fig 7b,c)。 尽管在C42B和22Rv1的CDK12 KO克隆中,CDK6和CDK14表达上调(Extended Data Fig 7d),但大多数其他CDK成员并未受到明显影响(Extended Data Fig 7d, e, 8a)。已知CDK12通过在RNA聚合酶II(RNA polymerase II,RNAPII)羧基末端结构域的丝氨酸2位点(Ser2)进行磷酸化来调控转录,并参与转录延伸和终止过程。CDK12敲除后,RNAPII Ser2位点的磷酸化水平(pSer2)在总蛋白及染色质结合蛋白组分中均出现轻度下降(Extended Data Fig 8b),提示转录过程受到轻微损害。 随后,在PCAWG和Hartwig队列中分析了SV断点相对于蛋白编码基因转录起始位点(TSS)和转录终止位点(TTS)的位置分布。结果显示,仅大型TD,而非其他类型SV在TTS附近显著富集(Extended Data Fig 8c),提示TRC及大型TD的形成可能与转录终止受损及RNAPII释放障碍密切相关。 已有研究表明,R环(R-loops)在基因组不稳定性中发挥重要作用,尤其是在DNA复制和双链断裂修复过程中;R环水平升高会阻碍转录和复制的顺利进行。结果发现,在22Rv1和C42B细胞中,CDK12缺失显著增加了整体R环水平(图5b–d,“TetRH − Dox”条件)。随后,研究人员采用近邻连接分析(proximity ligation assay,PLA),检测pSer2-RNAPII与DNA复制蛋白PCNA的共定位情况,以直接评估TRC——这是R环作为复制障碍所引发的潜在后果。结果显示,在三种细胞系中,CDK12 KO细胞均表现出显著增强的PLA信号,表明TRC水平明显升高(图5e–g,“TetRH − Dox”条件)。 在CDK12 KO细胞中重新表达野生型CDK12,可有效逆转R环积累和PLA信号增强(图5c–g)。此外,在CDK12 KO细胞中诱导表达RNase H1后,R环和TRC水平均降低至与CDK12野生型细胞相当的水平(图5c,e–g,“TetRH + Dox”条件)。与此同时,CDK12 KO细胞还表现出复制压力升高的分子标志(Extended Data Fig 8d–f),包括RPA32磷酸化增强及RPA32焦点数量增加。为进一步验证CDK12的功能,还采用CRISPR干扰(CRISPRi)技术构建了CDK12敲低细胞,结果同样观察到TRC显著增加(Extended Data Fig 8g,h)。 综上所述,这些结果清楚地表明,CDK12缺失可在前列腺癌细胞及正常前列腺上皮细胞中诱导R环积累并显著增强转录–复制冲突。 5、CDK12的缺失可以直接导致大型TD的形成 为直接评估CDK12 缺失对基因组不稳定性的影响,将C42B细胞(包括CDK12敲除株和对照株)连续培养了一年(图6a),以提供足够时间促使体细胞结构变异(SVs)的积累。鉴于单个细胞很可能携带各不相同的SV组合,分别从敲除组和对照组中各挑选3个单细胞,并将其扩增为克隆。随后,对这6个单细胞扩增克隆进行了全基因组测序(WGS)。同时,对亲本细胞进行了更高深度(200×)的测序,以便去除任何可能已存在的SV。 结果显示,对照克隆中各类体细胞SV的数量为63–155个,而CDK12敲除克隆中为40–78个(图6b)。由于C42B本身是一株癌细胞系,而基因组不稳定性又是癌症的标志性特征,因此在长期培养过程中,对照细胞持续发生基因组不稳定并逐渐积累体细胞SV是可以预期的。在对照克隆3中,观察到其体细胞SV数量明显高于其他对照克隆(图6b),这很可能源于其携带了FANCM基因的一个特异性有害突变(Extended Data Fig 8i);FANCM是Fanconi贫血通路中的关键组分。 尽管6个敲除和对照克隆之间SV的类型及总数量存在一定差异,但大型TDs)在各克隆中的比例相对稳定(图6c)。值得注意的是,CDK12敲除克隆中大型TD所占比例显著高于对照克隆:敲除克隆平均为15.2%,而对照克隆仅为4.7%(图6c)。这些结果表明, CDK12的缺失可直接促进大型串联重复的形成,从而加剧特定类型的基因组结构异常。 Fig. 6 Loss of CDK12 promotes large TD formation. 6、大型TD可以作为药物敏感性的生物标志物 鉴于CDK12 缺失细胞中TRCs显著升高,研究人员推测这类细胞可能更加依赖某些可被药物靶向的细胞通路。基于RNA测序数据,在C42B和22Rv1两种细胞系的CDK12敲除(KO)细胞中,G2/M检查点通路均呈上调状态(Extended Data Fig 7e),提示缺乏CDK12的细胞可能对G2/M检查点具有更高依赖性。然而,对C42B(Extended Data Fig 9a)和22Rv1(Extended Data Fig 9b)进行的细胞周期分析显示,在CDK12失活后,处于G2/M期的细胞比例反而下降,说明CDK12缺失对细胞周期的影响更为复杂,并非单纯增强G2/M阻滞。 随后,以大型TDs作为生物标志物,开展了一项无偏倚的计算机模拟(in silico)药物敏感性筛选。分析对象为癌症细胞系百科全书(Cancer Cell Line Encyclopedia,CCLE)中同时具有全基因组测序和药物筛选数据的203个细胞系。重点关注与DNA损伤、DNA损伤修复、DNA复制及转录相关的药物(补充表3),结果发现:大型TD高度富集的癌细胞系对两种药物显著更为敏感,分别是WEE1抑制剂MK-1775(亦称AZD-1775或adavosertib)和PARP抑制剂PJ-34(图7a)。 WEE1编码一种核激酶,可在S期识别DNA损伤并调控G2/M检查点转变,确保DNA修复完成后细胞才进入有丝分裂。在所有三种细胞系中,CDK12缺失均显著增强了对MK-1775的药物敏感性,同时也提高了对其他WEE1抑制剂(包括Debio 0123、ZN-c3和PD0166285)的敏感性(图7b–d、Extended Data Fig 10a–c)。在MK-1775处理后,CDK12 KO细胞中γH2AX染色水平明显升高,提示DNA损伤进一步累积(Extended Data Fig 10d)。 此外,由于CHK1和ATR位于DNA损伤信号通路中WEE1的上游,并共同参与G2/M检查点的激活调控,进一步测试了多种CHK1和ATR抑制剂。结果显示,CDK12 KO细胞对多种CHK1和ATR抑制剂(包括prexasertib、CHIR-124、AZD7762、CCT245737、ceralasertib、VX-970和VE-821)均表现出显著增强的敏感性(图7d、Extended Data Fig 10a–c)。 鉴于CDK12突变可诱导复制压力(Extended Data Fig 8d–f),而WEE1、CHK1和ATR抑制剂已知可引发异常的复制起始位点激活,因此,干扰DNA复制调控可能是这些抑制剂发挥作用的另一重要机制,但其具体分子细节仍有待进一步阐明。值得注意的是,研究还发现大型TD富集的癌细胞系对三种DNA合成抑制剂——苯达莫司汀(DNA烷化剂)、奈拉滨(鸟嘌呤类似物)和泛昔洛韦(另一种鸟嘌呤类似物)表现出耐药性(Extended Data Fig 10e)。 综上所述,研究表明,靶向DNA损伤信号转导因子或G2/M检查点,可能成为治疗CDK12缺陷肿瘤以及其他以大型串联重复高度富集为特征的癌症的一种潜在有效策略。 Fig. 7 Drug sensitivity 讨论: 本研究揭示了肿瘤中的大型TDs源于TRCs的积累及其修复失当。首先在三个相互独立的泛癌全基因组测序队列(PCAWG、Hartwig 和 POG570)中解析并提取了高度保守的体细胞简单结构变异(SV)特征。基于TRC形成的SV应表现出已复制链偏倚这一推断,确实在两种大型TD特征中观察到了显著的已复制链偏倚。该偏倚依赖于转录活动,且不能由其他任何基因组因素解释,并在两个泛癌队列以及多个独立队列中均可重复验证。此外,发现CDK12突变与前列腺癌和卵巢癌中大型TD的高度富集显著相关。在实验层面,进一步证明,敲除CDK12——这一RNA聚合酶II(RNAPII)介导转录的关键调控因子——会导致R环、TRC以及大型TD显著增加。 研究采用了与既往癌症突变链不对称性研究相似的方法来推断复制方向。图2a所示的左、右复制区域被定义为“锐利转变区(sharp transition regions)”,仅使用这些区域以确保复制方向推断的高可靠性。由于“平坦区(flat regions)”中的复制方向难以明确界定,且无法检验SV链偏倚,因此在本研究中未予采用。然而,这并不意味着TRC不会发生在平坦区。值得注意的是,在肿瘤中,大型TD在最早复制区域中最为富集(Extended Data Fig 2d,TD3和TD4在最左侧区域的峰值最高),提示TRC可能更频繁地发生于早复制区域。这与早复制区域富含转录活跃基因、从而更易发生TRC的事实相一致。 基于上述结果,研究人员提出如下模型来解释观察(图7e):在CDK12完全缺失的肿瘤中,RNAPII无法被正确磷酸化,从而导致转录过程受损,尤其是转录终止阶段受阻。当RNAPII不能及时从DNA模板上释放时,会形成R环,继而阻碍DNA聚合酶复合物和复制叉的推进。一旦发生TRC,其中绝大多数可被细胞正确修复;但在极少数情况下(约每个细胞每月一次),停滞的复制叉未能得到有效修复并发生坍塌。由此产生的染色体断裂会形成DNA双链断裂(DSBs),最终导致大型TD的形成。进一步地,一部分大型TD会扩增多个已知癌基因,因此这些大型TD可能受到正向选择,并在肿瘤发生发展中发挥促进作用(图7e)。 尽管如此,仍有若干关键问题尚待解答。例如,TRC究竟如何特异性地导致大型TD的形成。DNA损伤修复(DNA-damage repair,DDR)系统在SV形成中无疑发挥着重要作用。已有研究表明,BRCA1和BRCA2参与R环的解析过程。在CDK12缺失背景下,既往研究还发现CDK12通过调控内含子多聚腺苷酸化,控制包括BRCA1和ATM在内的多种DNA修复基因的表达。因此,CDK12缺失所引发的整体DDR功能缺陷,可能导致TRC修复异常。由此推测,CDK12缺失不仅可能直接促进TRC的发生,还可能削弱TRC的修复能力,从而在CDK12缺陷细胞中导致TRC持续积累。 另一个悬而未决的问题是:为何TRC会特异性地产生大型TD,而非缺失或易位等其他类型的SV。由DSB产生何种SV,取决于断裂DNA末端所选择的修复伴侣。例如,当断裂末端与其他染色体连接时,将形成易位。TRC产生TD这一现象提示,坍塌的复制叉可能向后折返,并与碰撞位点上游的修复伴侣连接。既往研究显示,在BRCA1突变背景下,停滞的复制叉可通过断裂–融合、微同源介导的断裂诱导复制(MMBIR)或复制重启–旁路三种机制形成小型TD。在癌症中,大型TD并不与同一位点的大型缺失共现,提示其更可能通过MMBIR或复制重启–旁路机制形成(图7e)。从进化角度看,对于无法在碰撞后有效重启复制的细胞而言,形成大型TD可能是最优解。由于TRC总是发生在基因内部,在每个碰撞位点,基因的一部分已被复制,而另一部分尚未复制。若形成缺失、倒位或易位等其他SV,将导致该基因无法完整复制,对细胞更为致命;而唯一能够保留基因序列完整性的方式,是对这些区域进行再次复制,从而形成TD。如果复制叉仅在碰撞位点附近向后折返形成小TD,DNA聚合酶很快会再次到达碰撞位点,若此时R环尚未清除,将引发更多冲突。因此,避免重复碰撞的最佳策略,是在距离碰撞位点上游数百千碱基处向后折返,使DNA聚合酶在到达碰撞位点时,RNAPII已被释放、R环得以解析,从而形成大型TD。 针对携带大型TD的肿瘤进行选择性治疗具有重要的临床潜力。既往研究提示,大型TD可能通过形成基因融合产生新抗原,从而被免疫系统识别。近期完成的一项Ⅱ期临床试验评估了针对CDK12突变的前列腺癌及其他癌症的免疫检查点治疗,但疗效有限。PARP抑制治疗亦已被探索,仍值得进一步研究。鉴于携带大型TD的肿瘤可能在TRC修复和DNA复制方面存在缺陷,进一步寻找由CDK12缺失引发的合成致死脆弱性。数据表明,多种DNA损伤信号转导和G2/M检查点蛋白(如WEE1、CHK1和ATR)在这一背景下可能是关键治疗靶点,而大型TD及CDK12突变有望成为预测药物敏感性的有吸引力的生物标志物。 END 阅读最新文献,紧跟前沿进展,这是一名研究者必须具备的习惯和要求。我们华西医院耳鼻咽喉头颈外科的硕士、博士研究生和博士后们自2019年以来,每周开展一次文献泛读和文献精读分享会,至今已累计开展了200多次。2023年9月13日开始,本科室陆续将其进行整理,同步推出在线前沿速递和文献解读板块。通过这种学习和分享的方式,使汇报者和大家都能对近期权威期刊发表的高质量研究有所了解,同时也是学习其他优秀研究者思路、方法和理论的良好手段。希望通过这种形式,把科内的分享扩大到所有的读者,一起学习,共同进步! 华西医院耳鼻咽喉头颈外科 2023年9月13日