精读分享│【JOURNAL OF EXPERIMENTAL & CLINICAL CANCER RESEARCH】:头颈部肿瘤类器官生物样本库:基于TP53/HPV状态建立个体化放疗反应预测模型
英文题目:Head and neck tumor organoid biobank for modelling individual responses to radiation therapy according to the TP53/HPV status
中文题目:头颈部肿瘤类器官生物样本库:基于TP53/HPV状态建立个体化放疗反应预测模型
期刊:JOURNAL OF EXPERIMENTAL & CLINICAL CANCER RESEARCH(IF: 12.8)
单位:德国法兰克福歌德大学、Georg-Speyer-Haus肿瘤生物学和实验治疗研究所等机构合作发表
发表时间:2025年3月



摘要:
背景:
头颈癌(HNC)是一组异质性极高的疾病,治疗结果难以预测。患者来源的肿瘤类器官(PDTO)为个体化治疗测试和深入了解主要HNC驱动因素提供了巨大的潜力。
方法:
该研究建立了头颈类器官生物库(HNOB),该生物库对TP53突变体和人乳头瘤病毒16型(HPV 16)感染驱动的HNC临床相关亚型进行了分子和功能表征。将类器官暴露于放疗,其反应与临床数据相关联。基因工程正常类器官和肿瘤类器官用于测试TP53缺失和HPV感染的直接功能后果。
结果:
生成了由18个类器官模型组成的HNOB,其中包括15个肿瘤模型。确定了亚型相关的转录组学特征和病理特征,包括MDM2抑制剂Nutlin-3对TP53稳定的敏感性。此外,描述了一种体外放射反应测定,揭示了与个体患者的治疗结果相关的表型异质性,包括复发概率。使用基因工程类器官,证实了两种癌症驱动因素共存的可能性。TP53缺失以及HPV感染均促进了正常和肿瘤类器官的生长。TP53功能丧失本身不足以促进辐射抵抗,而HPV 16癌基因E6/E7通过诱导细胞周期停滞介导放射敏感性。
结论:
该研究结果强调了头颈类器官模型的转化价值,不仅对患者分层具有重要意义,而且对特定癌症驱动因素的治疗反应性的机制验证具有关键作用。
研究思路及方法:
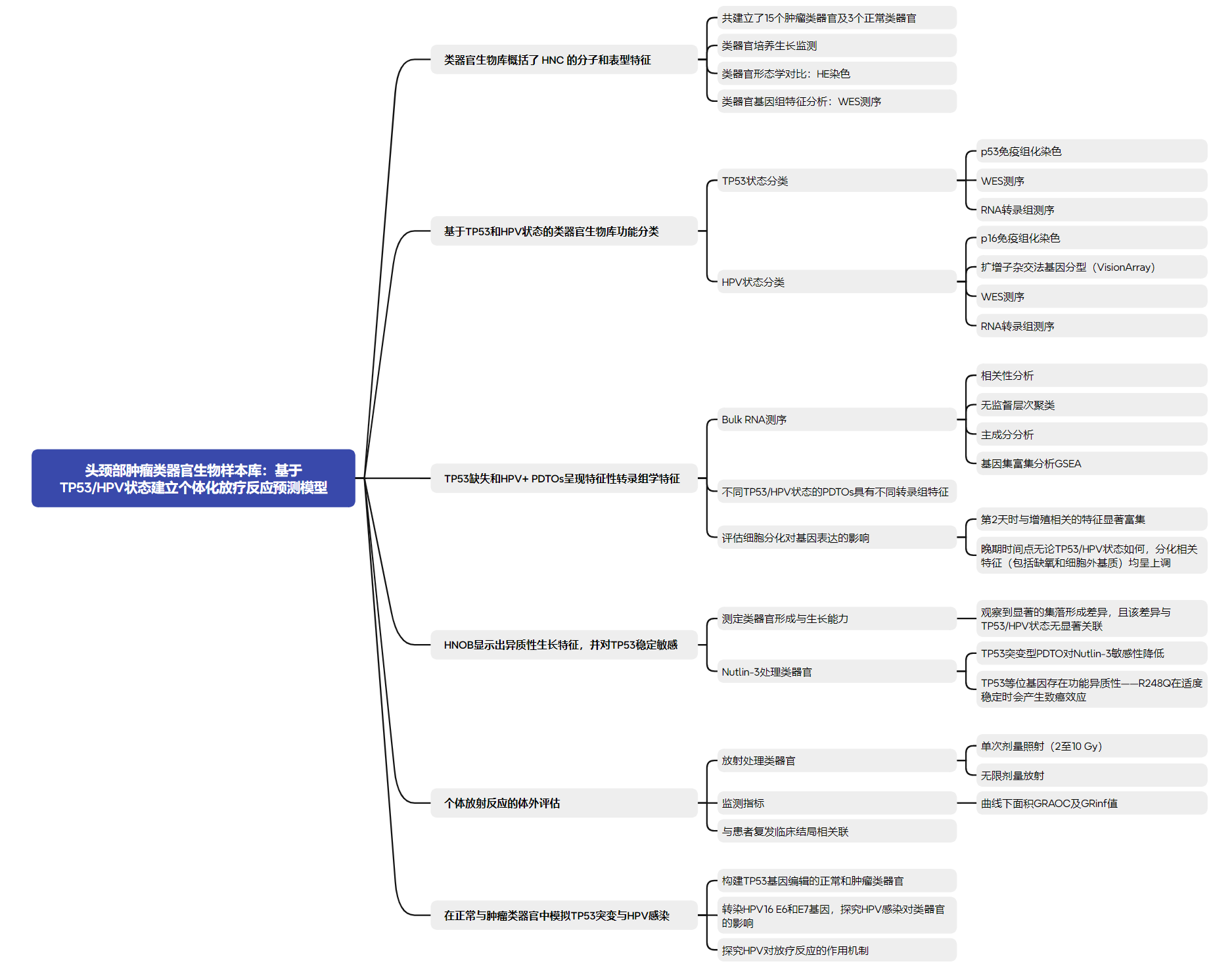
主要结果:
1.类器官生物库概括了 HNC 的分子和表型特征
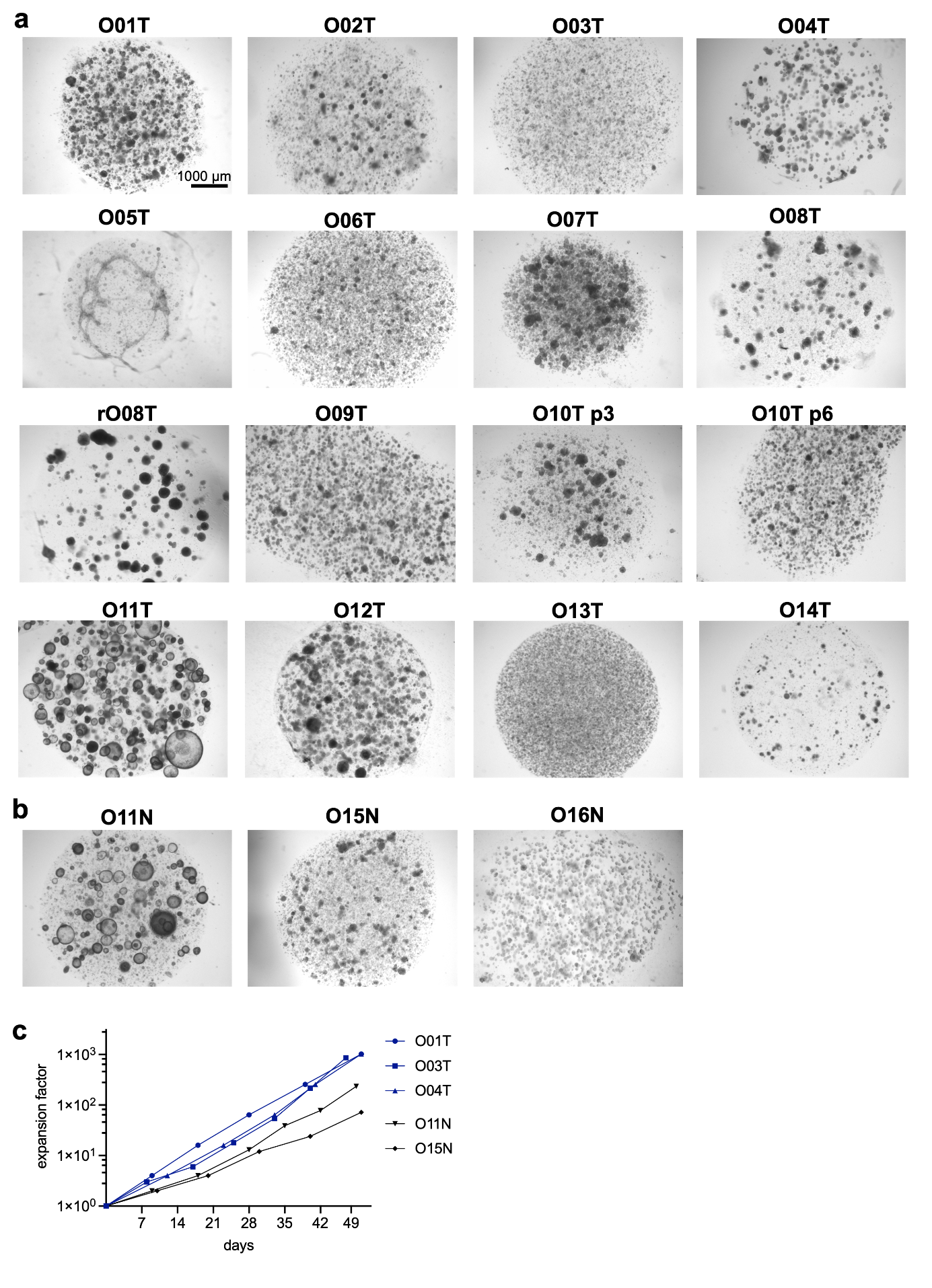
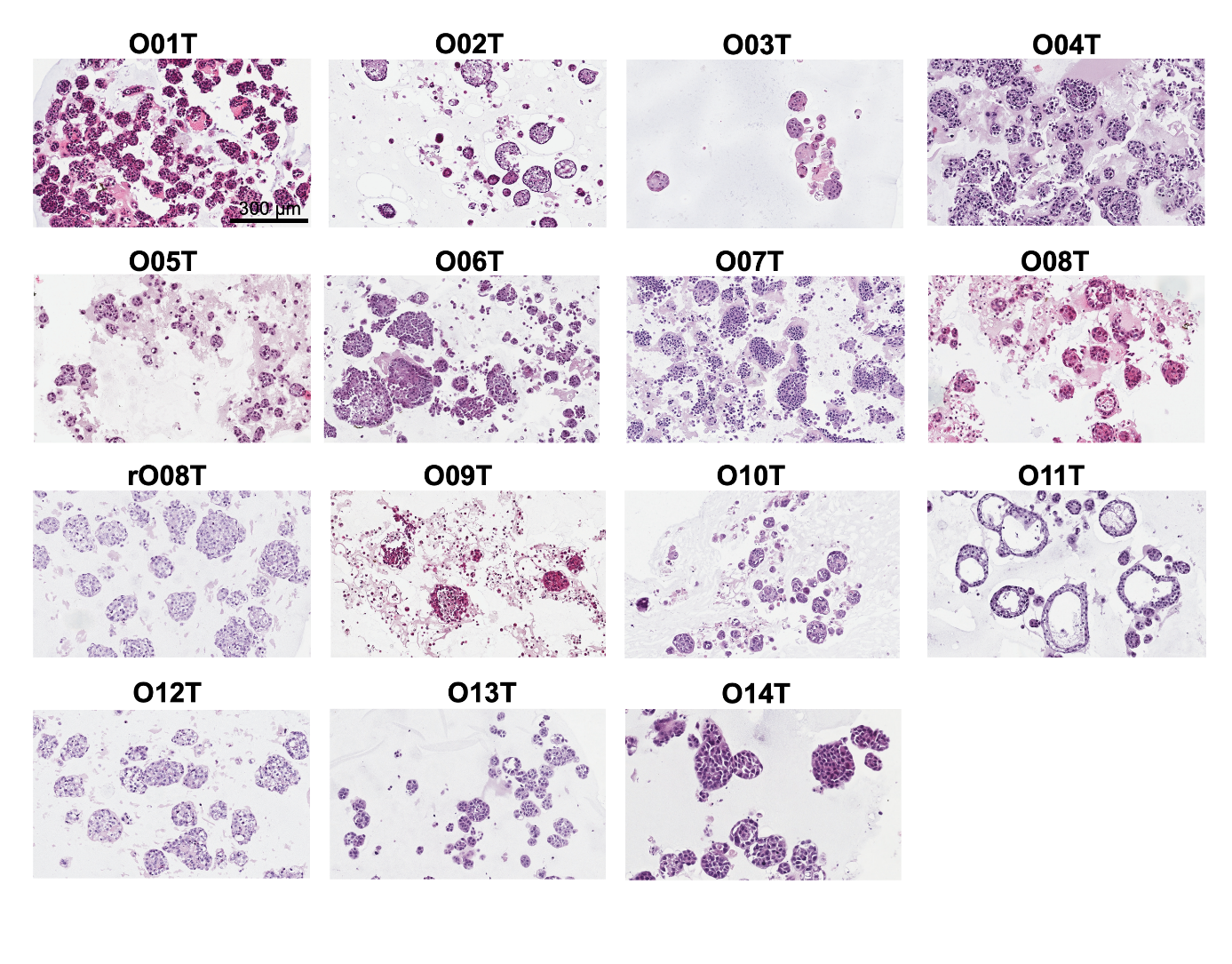
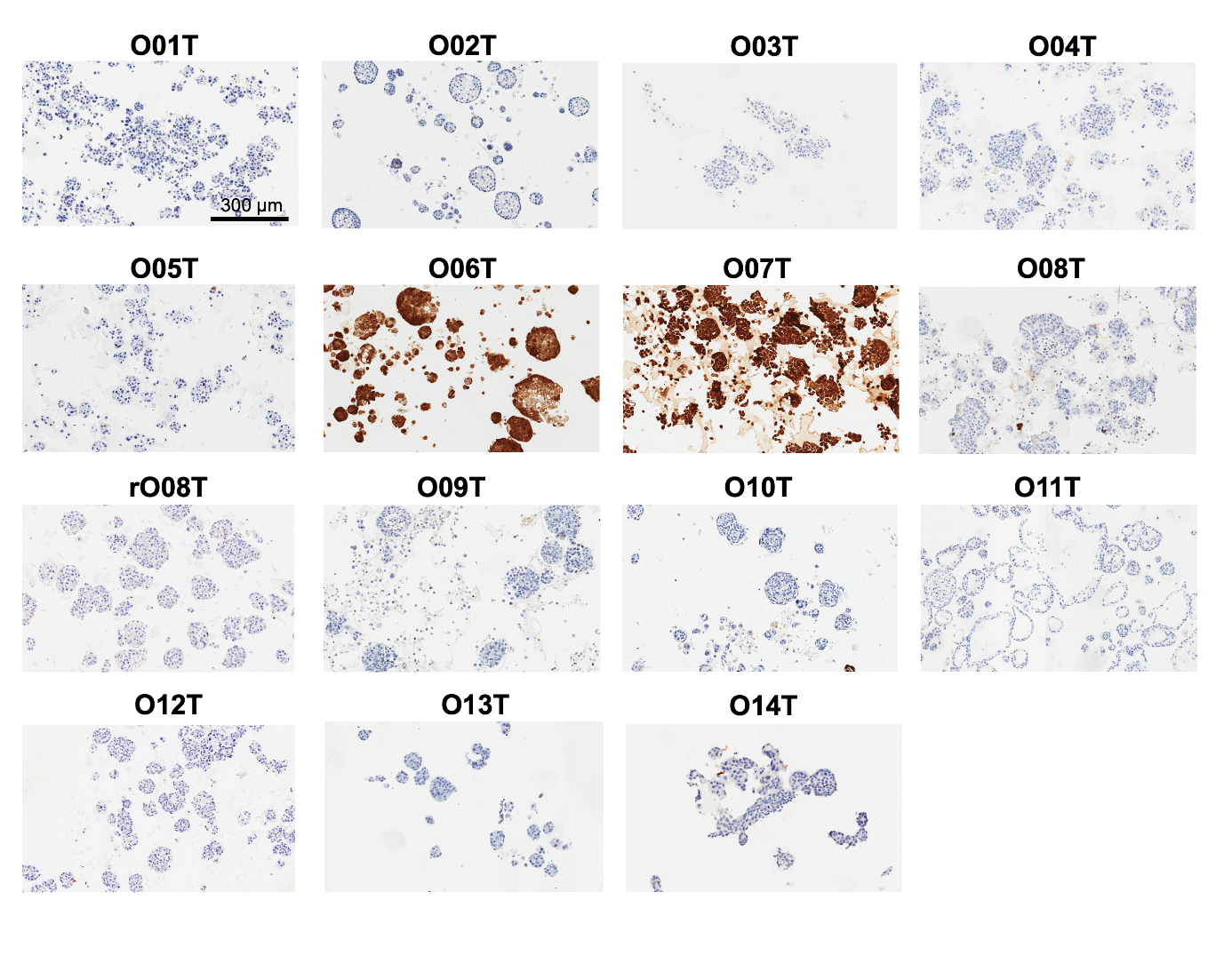
为建立头颈部类器官生物库(HNOB),该研究从14名患者(8男6女)中建立了15个肿瘤类器官,这些患者处于不同病期、具有不同实体类型和病灶部位,涵盖了主要头颈部鳞状细胞癌亚型。其中一个PDTO(O02T)源自腺癌(Fig. 1a, b; Supplementary Fig. S1a)。rO08T源自舌癌早期复发病例,该病例在接受舌部部分切除术后三个月复发,且未对原发肿瘤O08T进行辅助治疗。除经新辅助化放疗(CRTx)后采集的O12T外,其余所有类器官均通过术前未接受治疗的标本经手术切除获得。此外,从切除标本中未受影响的肿瘤邻近区域成功建立三个正常类器官系(Supplementary Fig. 1b)。采用Driehuis等(2019)优化的培养条件,类器官可实现长期扩增(>15代)。类器官呈现指数增长,平均每7-14天传代一次(Supplementary Fig. S1c)。除O11T和O11N呈现囊性表型外,其余均保持特异性形态学特征,主要表现为致密上皮结构(Fig. 1c; Supplementary Fig. S1a, b; S2)。
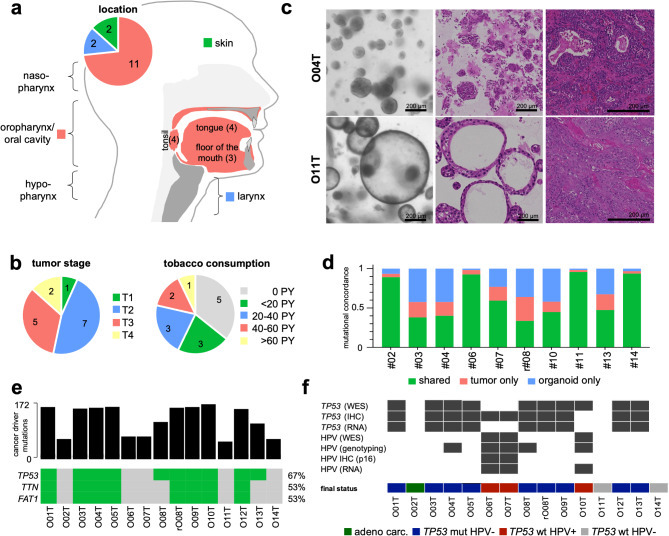
Figure 1. Clinical and genetic characteristics of head and neck cancer organoid biobank.
Figure S1. HNSCC organoid morphology and expansion.
Figure S2. Hematoxylin and eosin staining of HNSCC organoids.
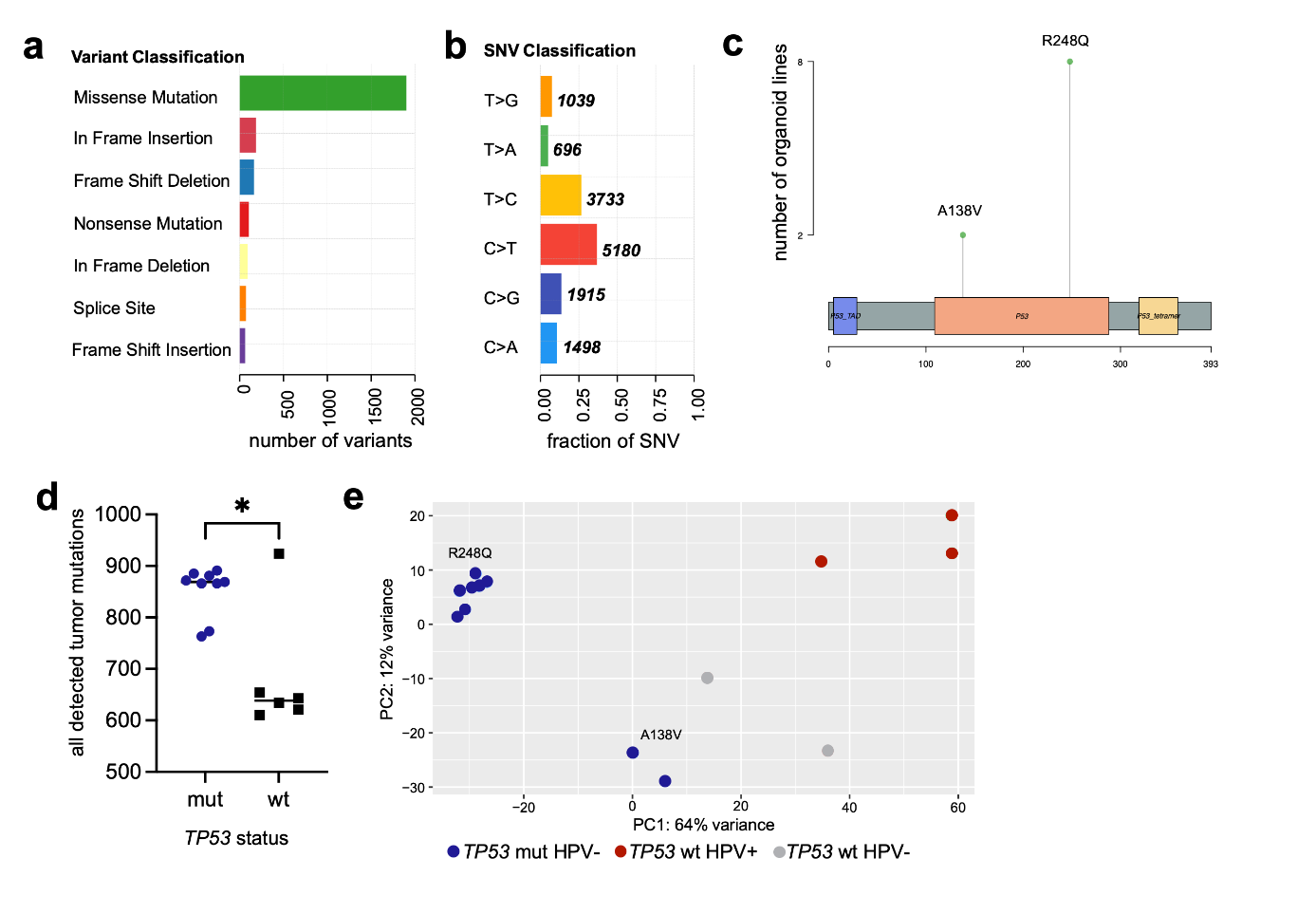
为进行基因组特征分析,对10份PDTO样本及其对应肿瘤组织进行了全外显子组测序(WES)。PDTO与肿瘤组织间单核苷酸多态性(SNP)的比对显示整体一致性良好(63.4±26.2%),其中肿瘤特异性SNP占比(13.3±9.2%)与PDTO特异性SNP占比(23.2±18.1%)相当(Fig. 1d)。总体而言,多数检测到的变异为影响C>T转化的错义突变(Supplementary Fig. S3a, b),这与先前对HNSCC的研究结果一致。复发性突变的检测证实了已知驱动基因的存在(Fig. 1e)。如预期所示,TP53是突变频率最高的基因(15个PDTO样本中有10个携带突变)。检测到两种常见功能缺失变异:TP53R248Q(存在于O01T、O03T、O04T;O05T、rO08T、O09T、O10T、O12T及O13T)和TP53A138V(存在于O08T和O13T)(Supplementary Fig. S3c)。R248Q突变影响DNA结合区域,导致p53四聚体无法激活靶基因。TP53A138V则为罕见且临床报道较少的变异。TTN和FAT1突变(15例中有8例)始终与TP53突变共同存在。这三种突变均与高危亚型头颈鳞状细胞癌相关。根据TP53状态,检测到的肿瘤突变存在显著差异(p=0.033),这与p53在维持基因组完整性中的关键作用相符(Fig. 1e; Supplementary Fig. S3d)。与之相符的是,将两个类器官系O08T与早期复发系rO08T进行并列比较时,检测到的突变数量显著增加。一致性分析显示O08T与rO08T之间存在33.2%的共享突变。O08T具有29.5%的专属突变,rO08T则具有37.3%的专属突变,表明治疗过程中发生了遗传学转变。
Figure S3. Characterization by whole exome sequencing (WES) and RNA sequencing.
2.基于TP53和HPV状态的类器官生物库功能分类
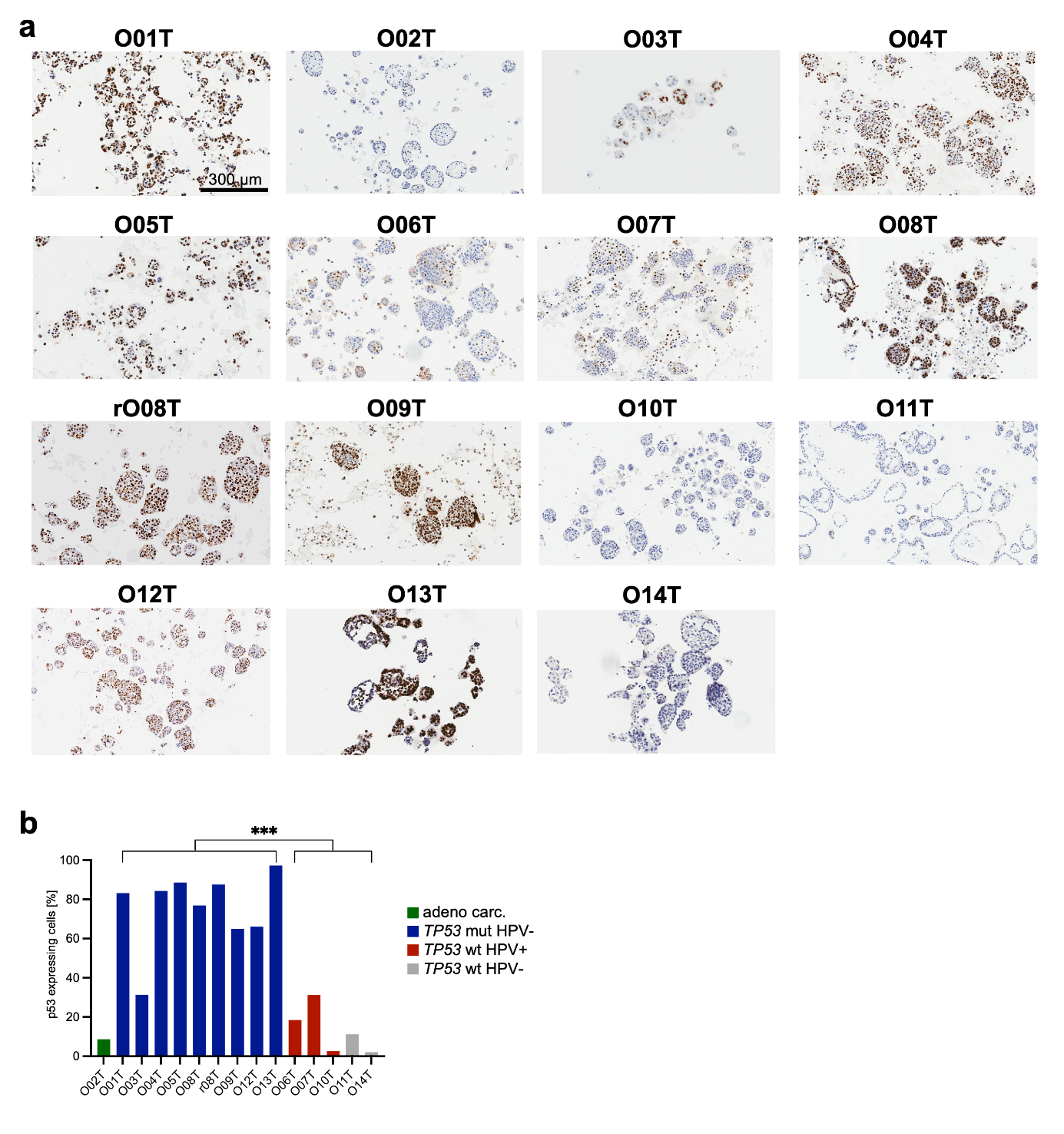
为确保病理亚型分类的一致性,根据TP53和HPV状态对PDTO样本进行分析。p53免疫组化染色显示11例PDTO呈阳性,其中10例经全外显子组测序(WES)验证(Supplementary Fig. S4a)。与TP53野生型PDTO相比,TP53突变型PDTO的p53染色水平显著更高(Supplementary Fig. S4b)。通过WES检测到的TP53突变在9份PDTO样本中有8份得到转录组水平验证(Fig. 1e, f; Supplementary Fig. S3e)。在O10T细胞系中,第3代培养物经WES检测发现TP53突变,但第6代培养物经p53免疫组化及RNA测序未能确认该突变,表明长期培养过程中发生基因型漂移并伴随表型改变(Fig. 1e, f; Supplementary Fig. S1)。
所有PDTOs的HPV状态通过替代标志物p16的免疫组化染色、扩增子杂交法基因分型(VisionArray)、全外显子组测序(WES)及RNA测序确定(Fig. 1f; Supplementary Fig. S5)。在组织中,扩增子杂交法可检测到HPV 16、HPV 33和HPV 35,但在PDTO中仅发现HPV 16,且所有来自正常邻近组织的类器官均为HPV阴性。值得注意的是,扩增子杂交法显示部分细胞系呈阳性,但免疫组化或测序无法确认,表明存在假阳性结果(Fig. 1f)。
综合分析结果,共分类出9个TP53突变型和3个HPV阳性PDTO,其发生模式如先前所述呈互斥关系。此外,另有两份PDTO(O11T和O14T)被归类为HPV阴性且TP53野生型(Fig. 1f)。这些结果表明,通过对肿瘤组织和PDTO进行组织学与分子学联合分析,可提高病理评估的准确性。
Figure S4. p53 immunohistochemistry of HNSCC organoids.
Figure S5. p16 immunohistochemistry in HNSCC organoids as HPV surrogate marker.
3.TP53缺失和HPV+ PDTOs呈现特征性转录组学特征
针对PDTOs的转录组测序采用批量RNA测序技术。相关性分析、无监督层次聚类及主成分分析揭示出TP53突变体(区分TP53R248Q与TP53A138V突变)与HPV+类器官的独立聚类(Fig.2a; Supplementary Fig.3e)。腺癌细胞系(O02T)与TP53R248Q突变体呈现相似性。未观察到基于解剖位置的聚类现象。随后对HPV阳性与TP53R248Q突变PDTOs进行差异基因表达分析(Fig.2b)。基因集富集分析(GSEA)显示,TP53突变与促炎标志性特征(TNF/NF-κB信号通路、补体激活、移植物排斥反应)及上皮间质转化(EMT)显著上调相关,这些特征与HNSCC更恶性的表型相关(Fig.2c)。此外,HPV阳性PDTOs呈现已知HPV特征性表达模式,包括KRAS信号通路下调(Fig.2d)及谷胱甘肽转移酶上调——该酶此前被报道为E7诱导的促生存程序标志物。
为评估细胞分化对基因表达的影响,在细胞分裂后第2天和第7天进行了RNA测序,随后进行差异基因表达分析(Fig.2e)。第2天时,基因集富集分析(GSEA)显示与增殖相关的特征显著富集(E2F靶基因、MYC靶基因、G2M检查点、干性及核糖体生物发生;Fig.2f)。相反,晚期时间点无论TP53/HPV状态如何,分化相关特征(包括缺氧和细胞外基质)均呈上调,表明HNSCC类器官具有显著的自发分化能力(Fig.2g)。
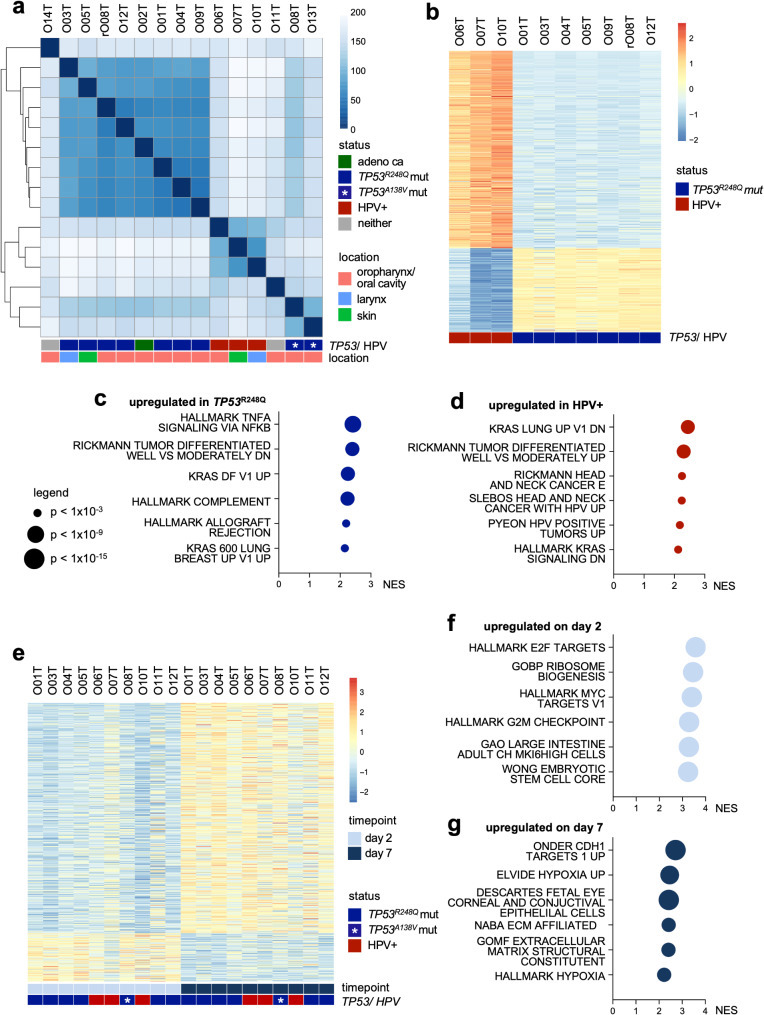
Figure 2. Transcriptomic characteristics of head and neck cancer organoid biobank.
4.HNOB显示出异质性生长特征,并对TP53稳定敏感
为进行功能表征,测定了类器官的形成与生长能力。在接种2000个单细胞并培养7天后,观察到显著的集落形成差异,且该差异与TP53/HPV状态无显著关联(Fig. 3a, b)。后续所有实验均对单细胞数量进行标准化处理,以获得可比性的类器官数量。通过144小时的RealTimeGlo™检测量化细胞增殖,结果显示各细胞系的细胞倍增时间相当(Fig. 3c)。由此证实,集落形成与生长能力属于亚型无关的特性。随后通过MDM2抑制剂Nutlin-3处理评估TP53活性。如预期,TP53突变型PDTO对Nutlin-3敏感性降低(Fig. 3d, e;p=0.004),验证了亚型分类结果。值得注意的是,低浓度和中等浓度的Nutlin-3在TP53R248Q PDTOs中反而导致ATP水平升高(Fig. 3d)。相反,TP53A138V PDTOs对Nutlin-3暴露表现出耐受性,但未出现ATP水平升高,表明TP53等位基因存在功能异质性——R248Q在适度稳定时会产生致癌效应。
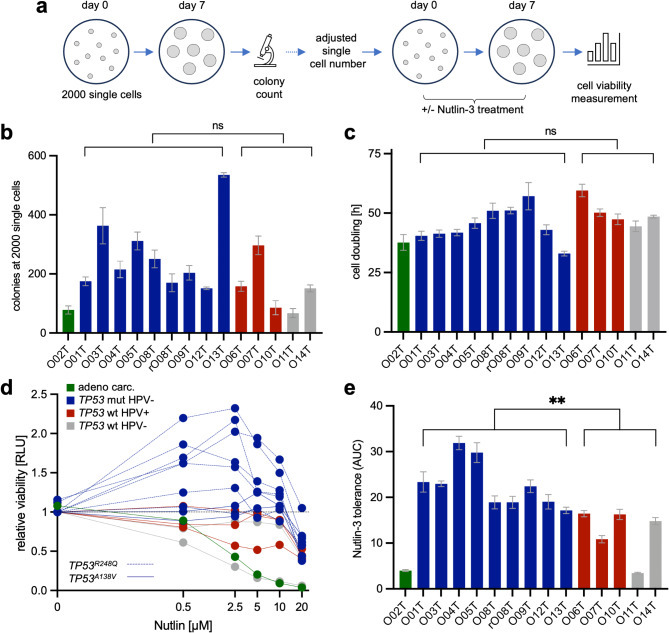
Figure 3. Phenotypic characterization of the head and neck cancer organoid biobank.
5.个体放射反应的体外评估
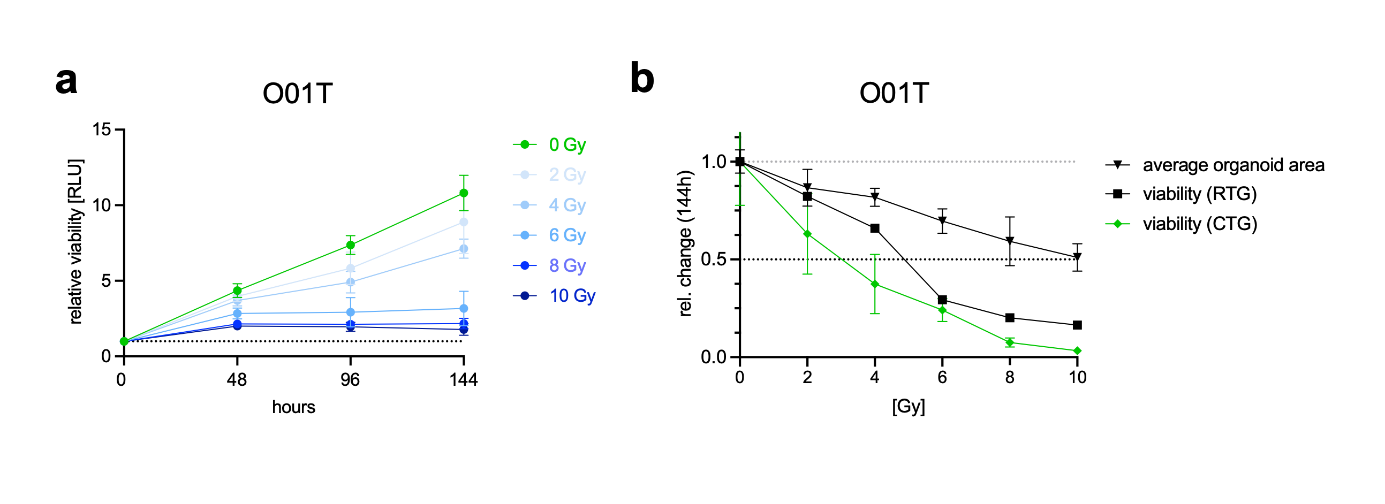
在临床实践中,头颈部癌症患者对放射治疗的反应存在高度异质性。亟需建立临床前检测方法来研究这些差异并开展个体化治疗试验。在HNOB模型中,通过单次剂量照射(2至10 Gy;Fig. 4a)评估了放射反应(RR)。采用RealTimeGlo®检测法监测细胞存活率,并通过生长速率(GR)指标计算各细胞系生长差异,该指标与终点测量结果高度吻合(Supplementary Fig. S6a, b)。观察到两种特征性表型:高剂量下完全应答的细胞系,以及低剂量部分应答但高剂量下持续存活的细胞系(Fig. 4b)。曲线下面积(GRAOC)的量化显示各细胞系存在显著差异(Fig. 4c)。其中腺癌PDTO表现出高辐射耐受性,与临床观察一致。肿瘤类型或解剖位置与GRAOC无显著关联。但在临床实践中,将细胞系简明分类为高响应与低响应仍具重要意义。为此,该研究测定了模拟无限剂量下的GRinf值(Fig. 4d)。15个PDTO中有6个呈现正GRinf值,表明高剂量下仍持续生长,该指标被用作高危病例的分类指标。在14例HNOB患者中,10例在原发手术切除后接受了辅助放疗/化放疗,其中两名患者(P01、P08)在研究期间出现复发,二者GRinf值均为阳性,故被正确归类为高危患者。其余在类器官模型中被判定为低反应性的肿瘤均得以完整切除,且保留了较大安全切缘。在所有被归类为良好反应者组别中,至少两年的随访期间均未出现临床复发。综上所述,该实验揭示了RR的显著异质性与其个体化临床结局相关,表明该检测具有个性化应用价值。
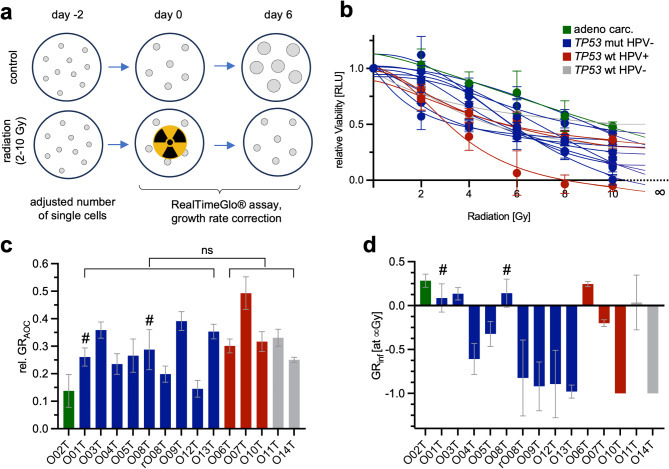
Figure 4. Radioresponse (RR) of head and neck cancer organoid biobank.
Figure S6. Characterization and validation of the radiation response (RR) assay.
6.在正常与肿瘤类器官中模拟TP53突变与HPV感染
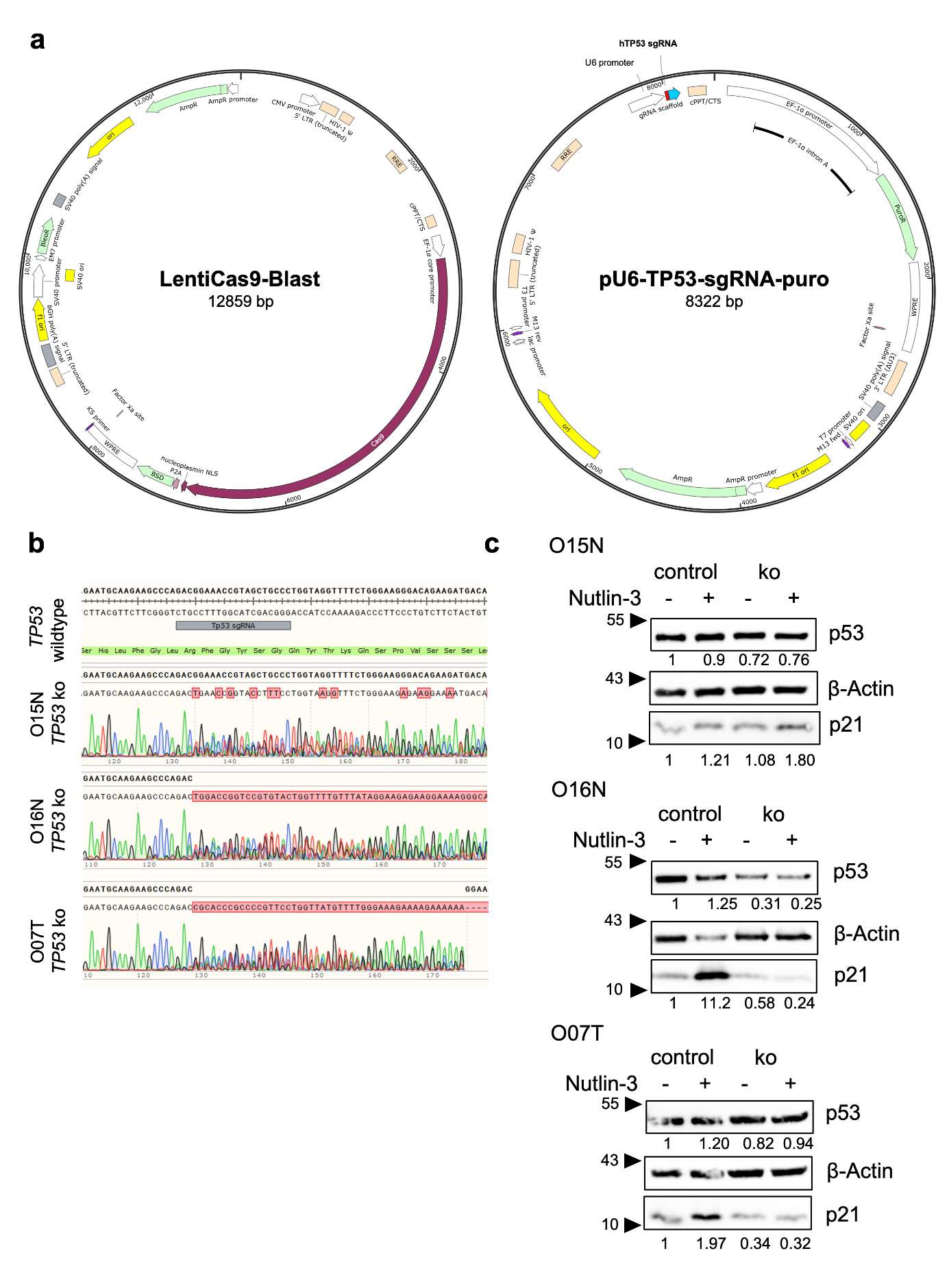
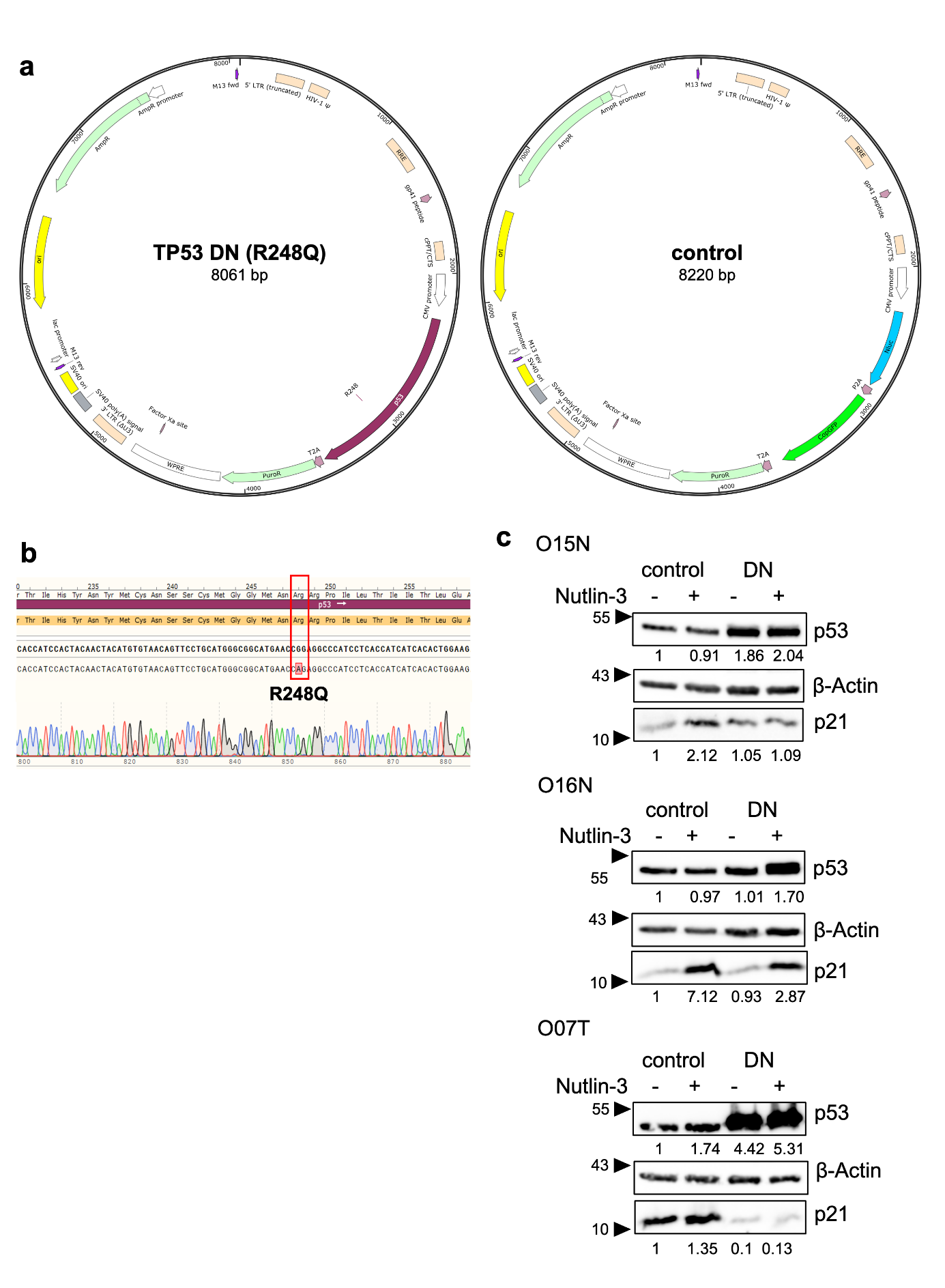
为研究肿瘤进展并评估TP53和HPV状态的直接影响,该研究建立了基因修饰方案。首先,在肿瘤邻近组织来源的正常类器官(O15N、O16N)以及TP53野生型且HPV阳性的肿瘤类器官(O07T)中研究了TP53缺失的影响。通过CRISPR/Cas9介导的基因敲除(Supplementary Fig. S7a)或慢病毒导入TP53失活突变体R248Q(Supplementary Fig. S8a)实现TP53功能缺失。经Nutlin-3筛选确认TP53功能丧失,并通过Sanger测序验证Cas9诱导的插入缺失突变(Supplementary Fig. S7b)。剂量滴定实验显示Nutlin-3耐药性(Fig. 5a, b)。Western blot分析表明,p53表达在过表达时增加,但在Cas9修饰细胞系中仅轻微降低,表明诱导了可能不影响蛋白水平的异质性突变(Supplementary Fig. S7c, S8c)。然而Nutlin-3处理后p53靶基因p21的诱导水平降低,表明该通路存在功能缺陷。TP53缺失的正常类器官单细胞形成集落能力显著强于对照系(Fig. 5c, d)。多数肿瘤及正常类器官的细胞倍增时间均显著短于对照系(Fig. 5e, f)。GRAOC在正常与肿瘤类器官中均轻度下降,表明仅TP53缺失不足以赋予辐射抵抗性(Fig.5g, h)。
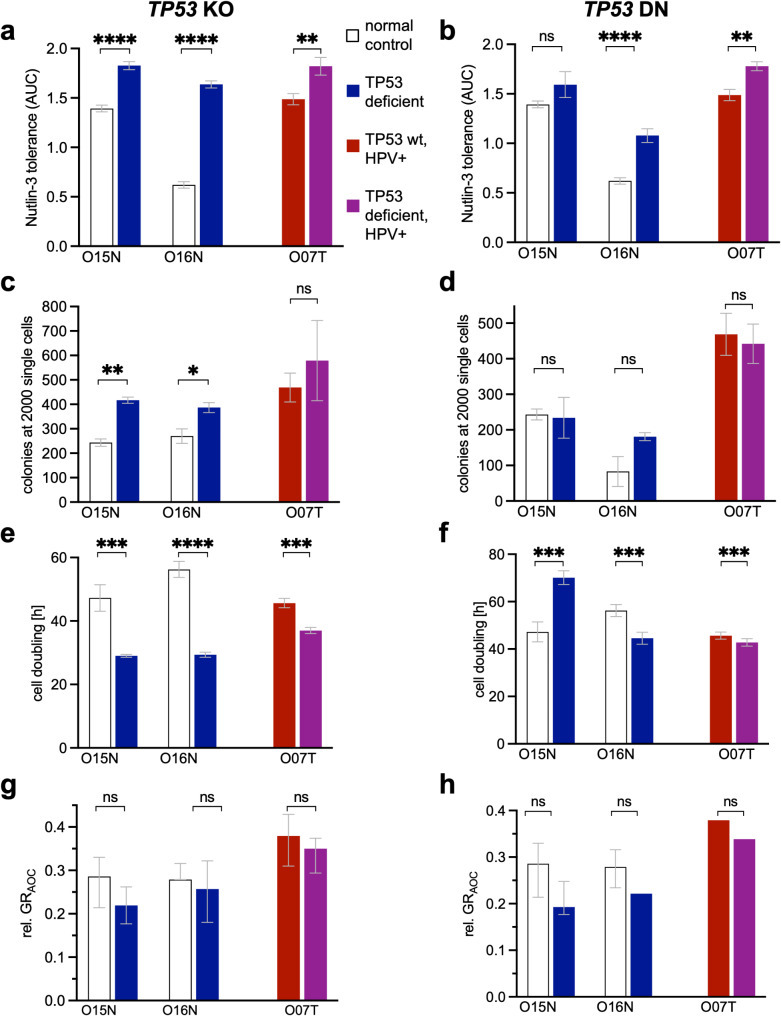
Figure 5. Genetic TP53 perturbations promote Nutlin-3 resistance and cell growth.
Figure S7. Modelling the TP53 status by CRISPR/Cas9 knock out in normal and tumor head and neck organoids.
Figure S8. Lentiviral expression of a dominant negative TP53 variant in normal and tumor head and neck organoids.
为探究HPV感染的表型后果,采用慢病毒策略(Supplementary Fig. S9a)将高危型HPV 16的致癌基因E6和E7导入两条HPV基因分型阴性的正常组织类器官系(O11N、O15N)。此外,采用TP53突变型(HPV阴性)肿瘤类器官(O04T、O08T、O09T)研究两种驱动基因共同存在的效应——此前研究表明这两种基因极少同时存在。通过RNA测序验证了E6/E7的过表达。与正常类器官不同的是,在三种肿瘤类器官中有两种,E6/E7显著促进了其集落形成(Fig. 6a)并缩短了细胞倍增时间(Fig. 6b)。E6/E7表达后类器官体积普遍增大(p=0.052)(Fig. 6c)。Nutlin-3敏感性未见一致性改变(Fig. 6d),表明E6介导的TP53不稳定化机制在口腔上皮原代细胞中不具主导作用。然而,与TP53状态工程化观察结果相似,E6/E7过表达证实了两种驱动因子可能同时存在的可能性。
接下来,该研究探究了HPV对RR的影响。剂量滴定显示,正常细胞系及3个肿瘤细胞系中的2个均呈现显著增强的敏感性(GRAOC)(Fig. 6e,f)。为探究其作用机制,通过PI/Hoechst染色及共聚焦成像测定了活/死细胞比例(Supplementary Fig. S9b, S9c)。经6 Gy单次剂量照射后,观察到E6/E7表达与正常细胞(O11N)和肿瘤类器官(O08T)中死亡细胞比例的持续增加相关,或导致O04T细胞在辐射暴露中的恢复能力明显下降(Fig. 6g)。仅在E6/E7表达未赋予放射敏感性的O09T细胞中,未观察到细胞死亡的明显影响。随后通过DAPI和KI67免疫染色结合流式细胞术分析细胞周期分布(Supplementary Fig. S9a-d)。在无辐射条件下,E6/E7表达细胞系未见细胞周期变化。然而,经6 Gy辐射24小时后,辐射敏感细胞系的G2期细胞比例显著升高(Fig. 6h)。辐射后72小时及120小时,所有细胞系均恢复至基线细胞周期分布,表明存在由E6/E7介导的暂时性G2期阻滞。
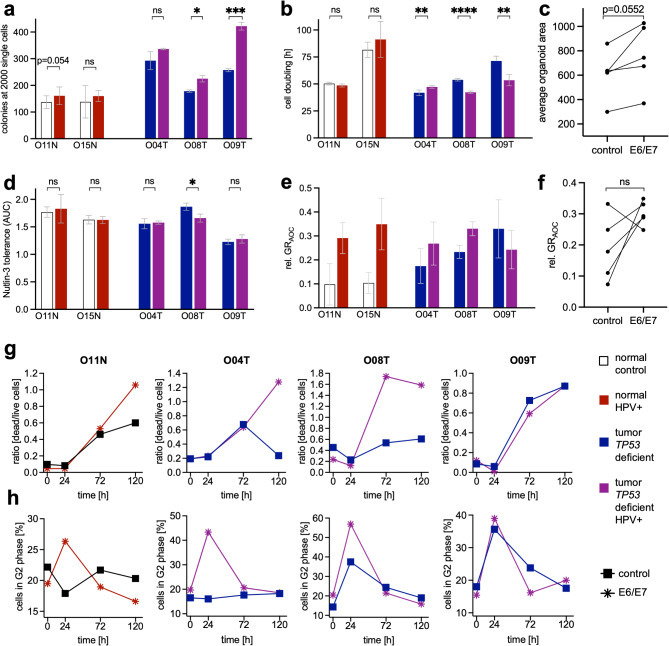
Figure 6. Modelling HPV by lentiviral E6/E7 expression induces cell growth and radiosensitivity.
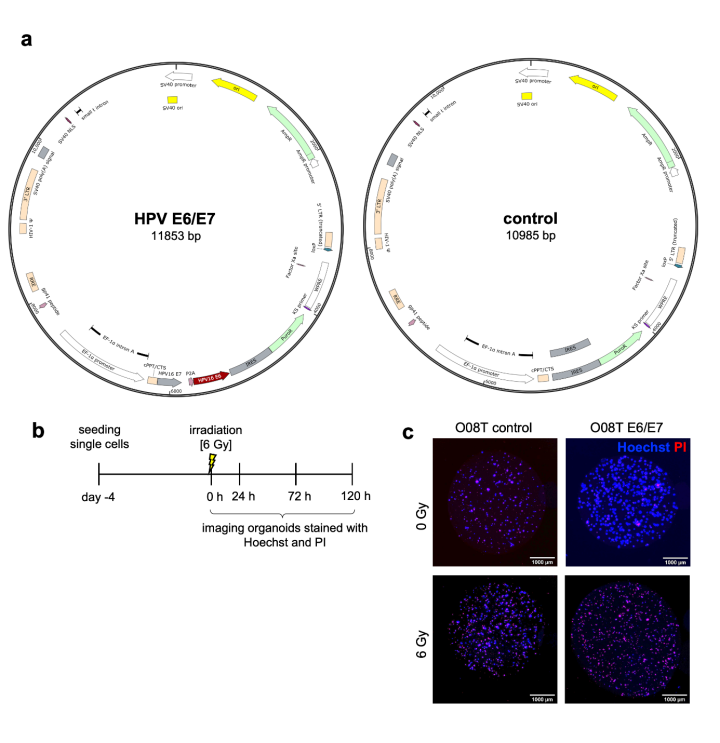
Figure S9. Modelling HPV status by E6/E7 overexpression in normal and tumor head and neck organoids.
汇报人:张宇阳
导师:赵宇
审核:厚媛、胡延昇、任建君