精读分享│:YTHDC1蛋白的乳酸化修饰调控其相分离行为,进而增强靶标mRNA稳定性并促进肾细胞癌进展
英文题目:YTHDC1 lactylation regulates its phase separation to enhance target mRNA stability and promote RCC progression
中文题目:YTHDC1蛋白的乳酸化修饰调控其相分离行为,进而增强靶标mRNA稳定性并促进肾细胞癌进展
期刊:Molecular Cell(IF=16.6)
单位:首都医科大学

Abstract
The hypoxic and lactate-enriched microenvironment of renal cell carcinoma (RCC) provides favorable conditions for aberrant lysine lactylation (Kla). However, the functional role and mechanistic basis of Kla in RCC progression remain elusive. Here, we showed an elevated global Kla level in human RCC tissues and cells, which promoted RCC malignancy. Through lactylome analysis of human RCC cells under hypoxiamimicking conditions, we found that the m6A reader YT521-B homology (YTH) domain-containing (YTHDC1) is modified by Kla at K82. YTHDC1K82la, mediated by p300 under hypoxia, promotes RCC malignancy both in vitro and in vivo. Mechanistically, YTHDC1K82la increases YTHDC1 phase separation, leading to the expansion of nuclear condensates and safeguarding oncogenic transcripts BCL2 and E2F2 from degradation by the poly A-tail exosome targeting (PAXT)-exosome complex in human RCC cells. Our results demonstrated that augmented Kla advances RCC progression by modulating phase separation and thereby regulating the stability of YTHDC1 target genes.
摘要
肾细胞癌(RCC)的缺氧和乳酸富集微环境为异常赖氨酸乳酸化(Kla)提供了有利条件。然而,Kla在RCC进展中的功能作用和机制基础仍不明确。该研究发现,在人类RCC组织和细胞中,整体Kla水平升高,且促进了RCC的恶性进展。通过在模拟缺氧条件下对人类RCC细胞进行乳酸化修饰组学分析,研究者发现m6A阅读器YTH结构域蛋白1(YTHDC1)在第82位赖氨酸处发生Kla修饰。在缺氧条件下由p300介导的YTHDC1K82la修饰,在体外和体内实验中均能促进RCC恶性进展。机制上,YTHDC1K82la增强了YTHDC1的相分离能力,导致核内凝聚物扩张,并保护致癌转录本BCL2和E2F2在人类RCC细胞中免遭PAXT-外泌体复合物的降解。研究结果表明,增强的Kla通过调控相分离进而调节YTHDC1靶基因的稳定性,从而促进RCC进展。
研究背景:
乳酸作为糖酵解的副产物,会在细胞需要快速生成三磷酸腺苷(ATP)或处于缺氧状态时累积。这种积累可促进乳酸化修饰——一种新型的翻译后修饰。乳酸化修饰受到酰基转移酶(如p300、CBP、Tip60、KAT7、KAT8等,以乳酸化辅酶A为底物)和去酰化酶(组蛋白去乙酰化酶HDACs及sirtuins家族)的可逆调控。近期研究发现,丙氨酰-tRNA合成酶1(AARS1)和AARS2可直接以乳酸为底物催化乳酸化修饰。组蛋白的乳酸化修饰通过调控下游基因表达影响肿瘤进展。此外,非组蛋白同样会发生乳酸化修饰,通过调节其功能参与包括肿瘤在内的疾病进程。研究显示,乳酸化修饰可通过多种机制调控肿瘤血管生成、同源重组修复、铜死亡、内皮-间质转化及免疫调节等生物学过程。鉴于乳酸化修饰在疾病中的重要作用,进一步探索其对癌症的影响及分子机制具有重大潜力。
肾细胞癌(RCC)作为泌尿系统高发恶性肿瘤,发病率持续攀升。该疾病通常对放化疗不敏感,靶向治疗易产生耐药。与其他实体瘤类似,RCC的缺氧-高乳酸微环境为乳酸化修饰提供了理想条件。RCC中存在的伪缺氧表型(如VHL和FH基因突变可在常氧环境下驱动缺氧应答)会影响组蛋白乳酸化水平并促进透明细胞肾癌(ccRCC)进展。然而,非组蛋白乳酸化修饰在RCC进展中的具体作用和机制仍待阐明。
YTH结构域蛋白1(YTHDC1)作为YTH家族中唯一定位于细胞核的m6A阅读器,通过调控靶RNA的选择性剪接、核输出及稳定性影响肿瘤发生。最新研究表明YTHDC1可发生生物分子凝聚。该过程通过形成无膜区室,实现对染色质组织、转录、RNA加工及翻译等关键细胞功能的时空调控。这类凝聚物可通过液相分离(LLPS)形成,其驱动力来自固有无序区(IDRs)与核酸之间的弱多价相互作用。多种生理病理状态(包括肿瘤进展)均会受到生物分子凝聚的调控。
无膜细胞器的形成受转录、与RNA/DNA等生物分子相互作用及翻译后修饰的调控。例如,m6A修饰的MYC mRNA可促进YTHDC1核凝聚物的形成,从而保护其免于降解并调控急性髓系白血病(AML)进展。YTH家族的凝聚也受翻译后修饰调控:低O-连接N-乙酰葡糖胺化修饰可驱动YTHDF1/3进入应激颗粒,促进细胞从应激状态恢复。近期研究证实,DNA结合蛋白(如p53和cGAS)的乳酸化修饰能够减弱其液相分离能力。但RNA结合蛋白的乳酸化修饰是否影响相分离凝聚体仍属未知。
该研究系统揭示了缺氧调控的RCC乳酸化修饰谱,证实缺氧诱导的差异乳酸化蛋白在RNA加工通路中显著富集。更重要的是,研究者发现YTHDC1第82位赖氨酸的乳酸化修饰(YTHDC1K82la)通过改变其凝聚特性,选择性将致癌转录本BCL2和E2F2包裹于凝聚体内免受降解,从而促进RCC进展。靶向YTHDC1乳酸化修饰有望成为RCC的潜在治疗策略。
研究思路:
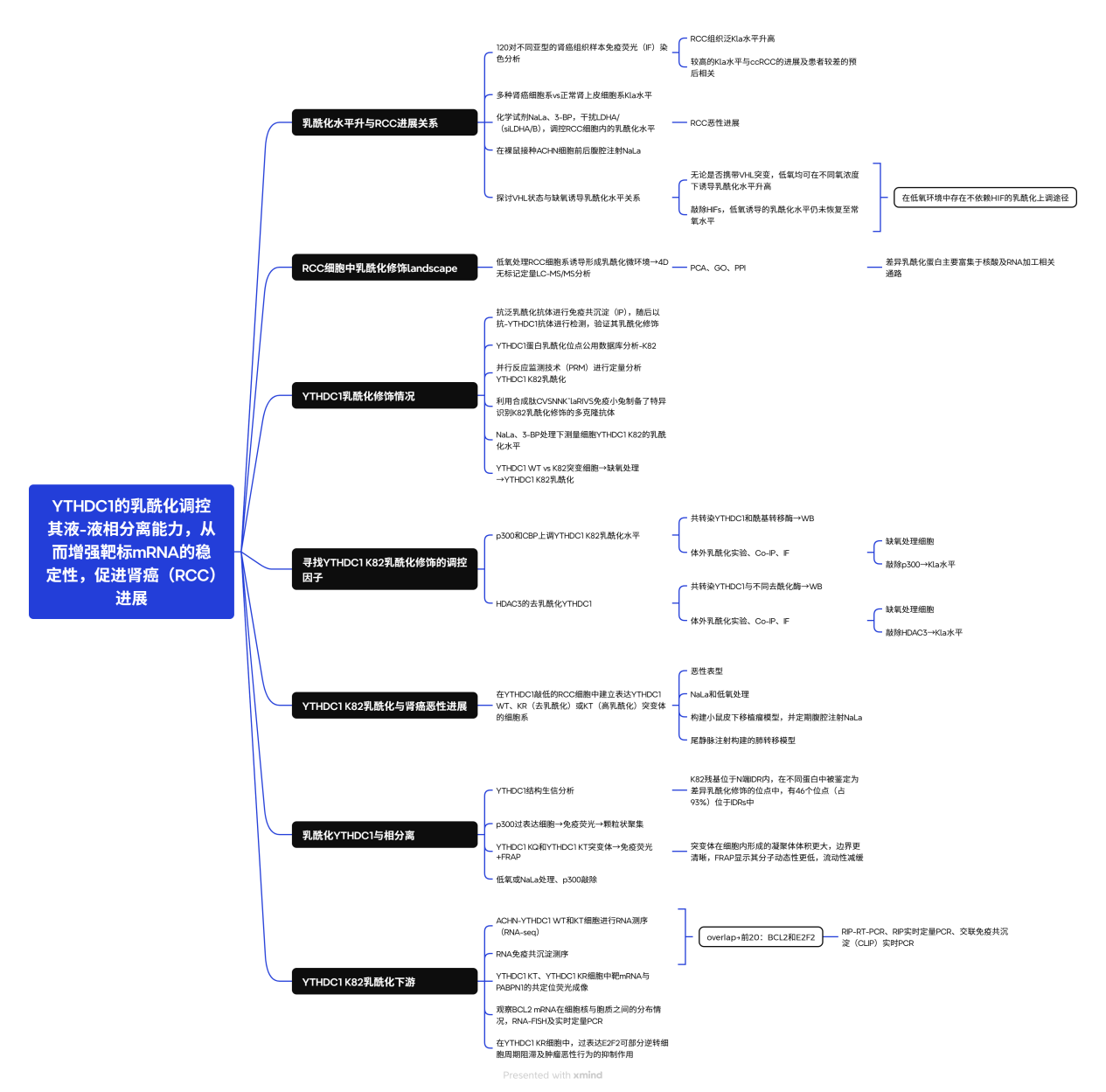
研究结果:
乳酸化水平升高促进肾细胞癌恶性进展
肾细胞癌细胞表现出增强的糖酵解活性,导致大量乳酸生成,为乳酸化修饰(Kla)提供底物。为此,研究者探讨了Kla与RCC的相关性。通过对120对不同亚型肾癌样本进行免疫荧光染色分析,研究者观察到RCC组织中泛Kla水平升高。此外,更高的总Kla水平与透明细胞肾癌进展和患者不良预后相关。与肾上皮细胞系相比,这一现象在不同肾癌细胞系中得到证实。这些数据表明,总Kla水平升高可能与RCC发展存在潜在关联。
为评估乳酸化对RCC发展的影响,研究者使用乳酸钠、糖酵解抑制剂3-溴丙酮酸(HK2抑制剂)及siLDHA/B调控RCC细胞内总Kla水平。重要的是,Kla水平的波动影响了RCC细胞的恶性表型。考虑到代谢通路干预除抑制乳酸产生和调节Kla水平外,可能对细胞产生次级效应,研究者尝试在3-BP和siLDHA/B处理的RCC细胞中直接补充乳酸钠以恢复Kla水平。该处理部分逆转了乳酸化抑制剂导致的RCC细胞存活和增殖能力下降。为研究乳酸化的体内效应,研究者在ACHN细胞接种前后对裸鼠进行腹腔乳酸钠注射。乳酸钠注射导致可触及肿瘤(约20 mm³)更早形成,并显著增加肿瘤体积。同时,乳酸钠注射组的乳酸化水平明显升高。这些发现表明,Kla水平升高可能在RCC细胞恶性进展中起关键作用。
包括RCC在内的大多数肿瘤在缺氧微环境中增殖。在缺氧条件下,多种RCC细胞系的Kla水平普遍升高,而其他酰化修饰(如乙酰化、巴豆酰化、丁酰化和琥珀酰化)在缺氧条件下并未升高。鉴于VHL突变在RCC中的重要性及其与缺氧诱导因子的密切关系,有必要研究VHL状态如何影响RCC中缺氧诱导的乳酸化。结果显示,对于VHL突变型和未突变型细胞,即使是在HIF1缺陷的769-P细胞中,乳酸化水平均在缺氧条件下以氧气浓度依赖性方式升高。值得注意的是,清除HIF后,缺氧诱导的乳酸化水平并未恢复至常氧水平,这证明了缺氧条件下存在一条不依赖HIF的通路来增加Kla水平。
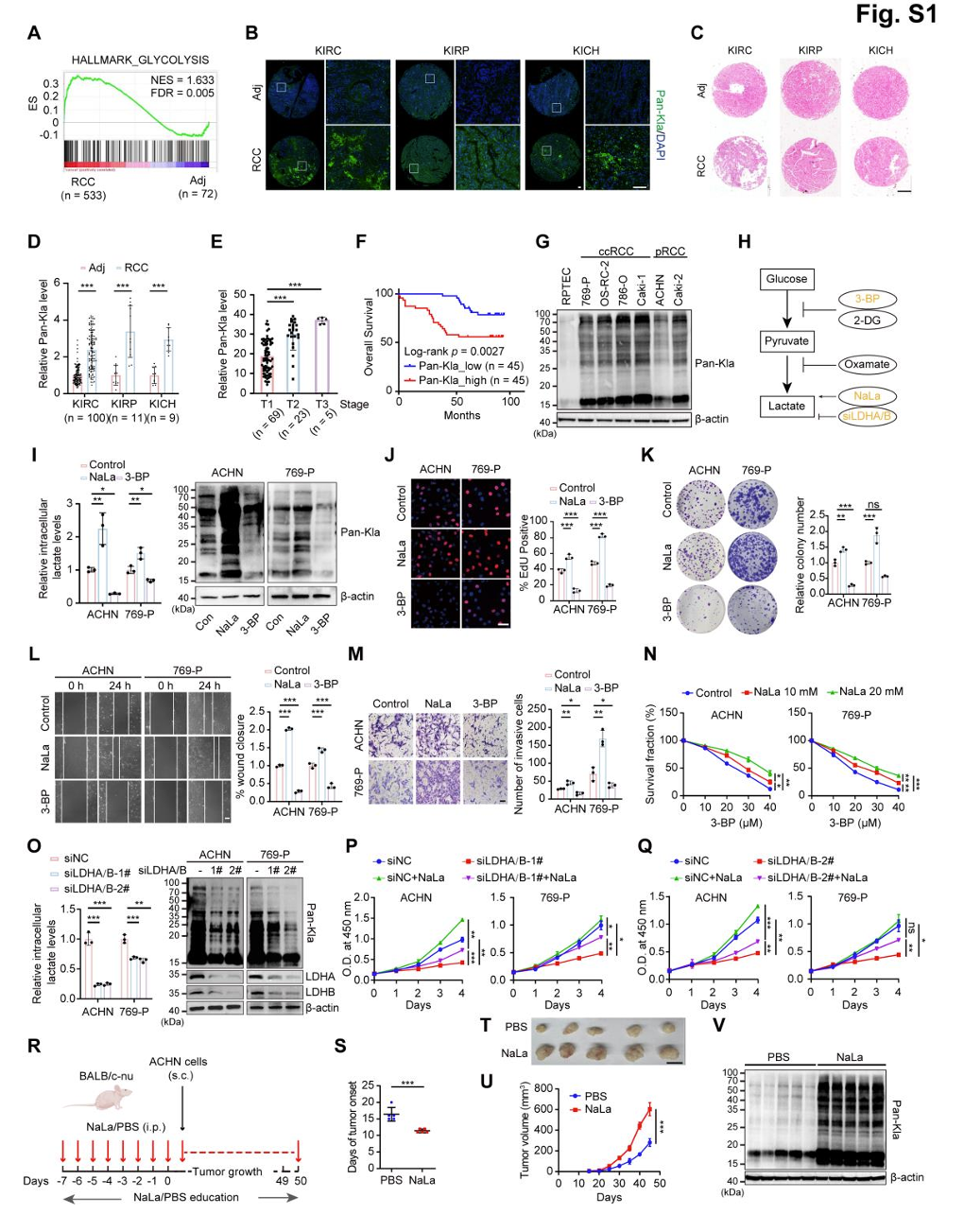
Figure S1. Elevated lactylation level promotes RCC malignancy, related to Figure 1, Table S1 and STAR Methods.
肾细胞癌细胞的乳酸化修饰全景图谱
为探索促进RCC进展的关键Kla蛋白,研究者采用缺氧处理诱导细胞乳酸化微环境。有趣的是,在RCC细胞中检测到跨越广泛分子量范围的多条蛋白条带,表明多种非组蛋白存在乳酸化修饰。与组蛋白类似,非组蛋白的Kla水平随缺氧处理时间延长而逐渐上调。为获取缺氧处理RCC细胞的乳酸化全图谱,研究者采用24小时缺氧处理诱导最大程度的高乳酸化蛋白,并进行蛋白质组与乳酸化修饰组检测。
结果显示蛋白质组和乳酸化修饰组数据集均具有优异的重复性,皮尔逊相关系数和相对标准偏差验证了数据可靠性。蛋白质组与乳酸化修饰组数据的主成分分析表明,常氧对照组与缺氧24小时组(H24组)样本分别形成独立聚类,且两组间分离明显。研究者严格执行样本质量控制,包括肽段长度分布、分子量分布及肽段数量评估。
蛋白质组分析成功定量5,195个蛋白,乳酸化修饰组分析定量370个蛋白及667个乳酸化位点。H24组与对照组间的差异表达蛋白分析鉴定出了74个上调和133个下调蛋白。这些差异表达蛋白广泛分布于多种细胞器。基因本体富集分析揭示了差异表达蛋白的潜在功能。
在H24组中,42个蛋白的49个乳酸化位点水平发生上调,未发现乳酸化水平下调的蛋白或位点。约70%和24%的差异乳酸化蛋白分别定位于细胞核和细胞质,表明缺氧诱导的乳酸化修饰主要作用于核内蛋白。环形图展示了蛋白质组与乳酸化修饰组分析的全景图谱。值得注意的是,差异乳酸化蛋白与差异表达蛋白无重叠,提示缺氧诱导的乳酸化可能不影响蛋白表达水平。蛋白质相互作用网络分析显示,差异乳酸化蛋白主要与核酸及RNA加工通路相关。直系同源蛋白簇分类和基因本体分析表明,差异乳酸化蛋白富集于RNA加工修饰等生物过程。这些结果提示乳酸化修饰与RNA相关细胞功能存在潜在相互作用。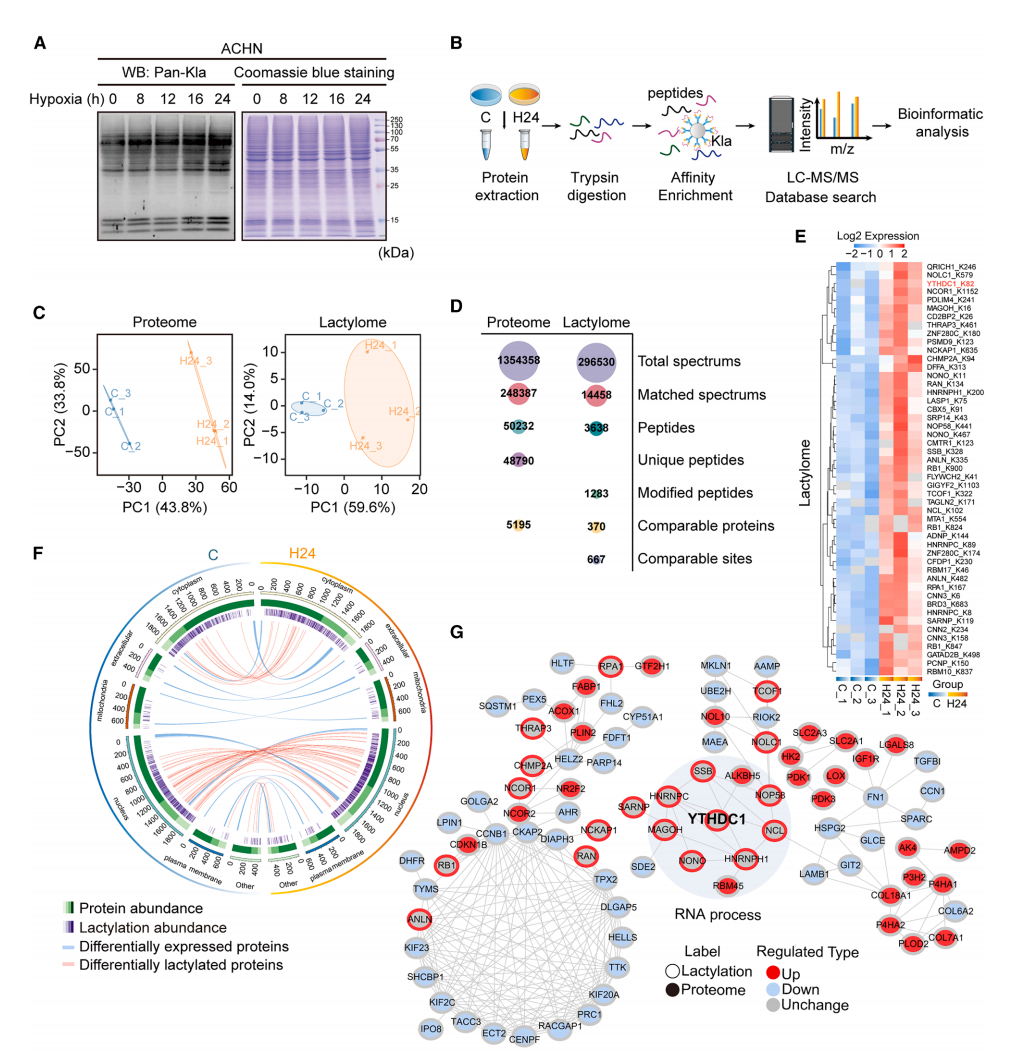
Figure 1. Comprehensive landscape of lactylation in RCC cells
YTHDC1K82在缺氧条件下发生显著乳酸化修饰
乳酸化的YTHDC1立即引起了研究者的关注,因为YTHDC1可通过结合靶标mRNA调控其选择性剪接、核输出、稳定性及降解,从而影响癌症进展。研究者通过泛乳酸化抗体免疫沉淀结合YTHDC1抗体检测验证了其乳酸化修饰。结果显示内源性YTHDC1(而非对照蛋白IGF2BP1,该蛋白在多个乳酸化组学数据中未检测到乳酸化修饰)可发生乳酸化。第82位赖氨酸(K82)是YTHDC1中唯一的乳酸化位点,该位点具有72.021 Da的质量偏移且在不同物种中高度保守。同时,研究者基于平行反应监测技术进行定量分析,发现K82的乳酸化比例约占YTHDC1总蛋白的0.60%。
为研究YTHDC1K82la水平的变化,研究者采用合成肽段C-VSNNKlaRIVS制备了特异性靶向YTHDC1第82位乳酸化赖氨酸的兔多克隆抗体。斑点印迹分析显示,抗体E17780能有效识别乳酸化肽段,而对乙酰化肽段及对照肽段无交叉反应。此外,将K82突变为R82(模拟去乳酸化状态)后,K82乳酸化水平显著降低,表明抗K82la抗体具有良好的特异性。值得注意的是,YTHDC1K82la水平在乳酸钠处理后升高,在3-溴丙酮酸处理后呈剂量依赖性下降,证实YTHDC1K82位点可发生乳酸化修饰。经过24小时缺氧处理,野生型YTHDC1(而非突变型)的乳酸化水平升高且呈现氧气浓度依赖性,说明YTHDC1K82la水平受到动态调控。
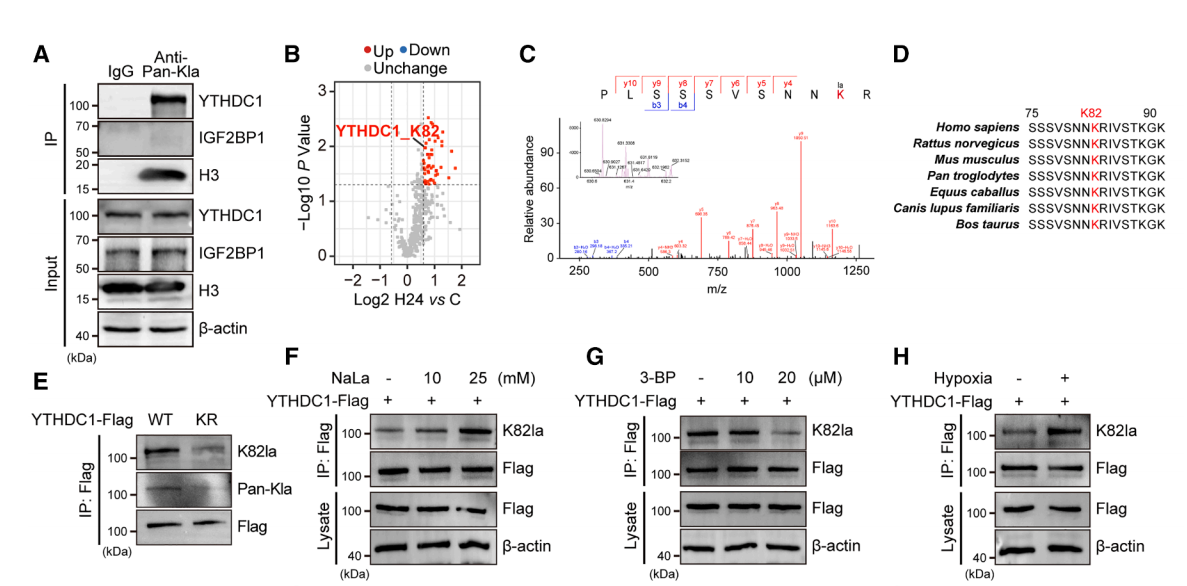
Figure 2. YTHDC1K82 is prominently lactylated under hypoxia, and its level is upregulated by enhanced interaction with p300
p300与HDAC3调控YTHDC1K82位点的乳酸化水平
组蛋白乳酸化修饰受酰基转移酶p300和去酰化酶HDACs调控,但这些酶是否调控YTHDC1乳酸化尚不明确。研究者的研究显示,p300和CBP均能增强YTHDC1K82la水平,而其他酰基转移酶如KAT8、KAT2B和KAT5对该位点无调控作用。体外乳酸化实验进一步证实p300介导的YTHDC1K82la水平上调。相反,敲低p300导致YTHDC1K82la水平显著降低。外源免疫共沉淀实验揭示p300与YTHDC1存在相互作用,免疫荧光显示p300与YTHDC1K82la具有共定位。此外,缺氧处理增强了YTHDC1与p300的相互作用,且敲低p300消除了缺氧条件下YTHDC1K82la水平的升高。这些发现表明p300能够感知细胞缺氧并催化YTHDC1K82乳酸化,该过程对缺氧应答至关重要。
为解析YTHDC1的去乳酸化酶,研究者使用HDAC抑制剂曲古抑菌素A(TSA)或sirtuins抑制剂烟酰胺处理HEK293T细胞。TSA处理后YTHDC1K82la水平升高,提示YTHDC1可发生去乳酸化且去乳酸化酶属于HDAC家族。通过共转染实验发现,过表达HDAC1-3(而非HDAC4-9)对YTHDC1K82具有去乳酸化作用,其中HDAC3效果最为显著。同时HDAC1-3与YTHDC1发生免疫共沉淀,表明去乳酸化作用依赖于蛋白互作。HDAC3过表达以剂量依赖性方式降低YTHDC1K82la水平,敲低HDAC3则提高其乳酸化水平。与p300不同,缺氧处理不影响HDAC3与YTHDC1的相互作用。这些数据表明,YTHDC1K82la水平受p300和HDAC3可逆调控,而缺氧通过增强p300与YTHDC1的相互作用促进YTHDC1K82la水平升高。
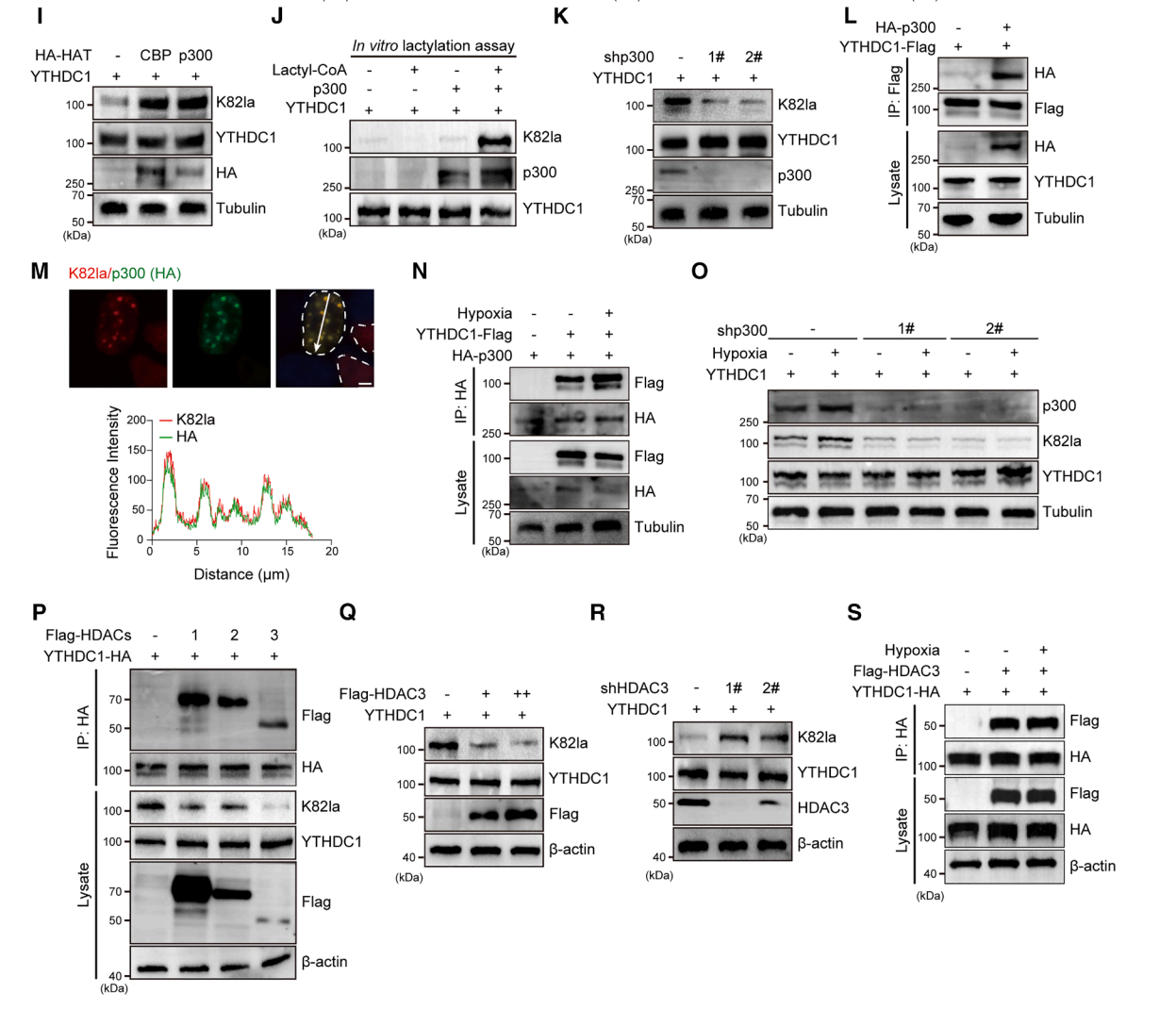
Figure 2. YTHDC1K82 is prominently lactylated under hypoxia, and its level is upregulated by enhanced interaction with p300
YTHDC1K82乳酸化修饰促进肾细胞癌恶性进展
由于乳酸化发生于赖氨酸残基,研究者将K82突变为精氨酸(YTHDC1KR,模拟去乳酸化状态)或苏氨酸(YTHDC1KT,模拟高乳酸化状态),并在敲低YTHDC1的RCC细胞中建立了稳定表达野生型及突变型YTHDC1的细胞系。与YTHDC1WT组相比,YTHDC1KT回补细胞表现出更多的S期进入和增强的恶性表型;而YTHDC1KR回补组则呈现更多G0/G1期阻滞及对RCC细胞恶性行为的抑制作用。额外添加乳酸钠和缺氧处理可调控YTHDC1WT回补细胞的增殖,但对YTHDC1KR回补细胞无影响。
为评估YTHDC1K82la对体内RCC恶性进展的影响,研究者进行了异种移植瘤实验。所有裸鼠均定期腹腔注射乳酸钠以建立体内高乳酸环境,提升肿瘤内YTHDC1WT的乳酸化水平。与ACHN-shYTHDC1-YTHDC1KR组相比,ACHN-shYTHDC1-YTHDC1WT组促进肿瘤生长,体积和重量分别增至243%和177%。此外,Ki67染色显示WT组的增殖能力强于KR组。在尾静脉肺转移模型中,注射ACHN-shYTHDC1-YTHDC1WT的小鼠出现恶病质和更明显的消瘦现象,剖检显示其肺转移灶(4/5)多于ACHN-shYTHDC1-YTHDC1KR组(1/5)。由于WT组多数转移灶隐匿于肺组织内部或相互融合,作者未对转移灶数量进行定量统计。这些结果证实YTHDC1K82la在促进RCC生长和转移中起关键作用。临床样本分析显示,RCC组织中YTHDC1K82la水平升高且与ccRCC患者不良预后相关,提示YTHDC1K82la在临床层面促进RCC恶性进展。
同时,YTHDC1KT回补细胞对靶向药物舒尼替尼的反应较差。额外添加乳酸钠、缺氧处理及p300抑制剂均未改变YTHDC1突变体的药物敏感性。在腹腔注射乳酸钠的异种移植瘤模型中,相较于单药治疗组,舒尼替尼与3-溴丙酮酸联合治疗在抑制肿瘤生长、减小肿瘤体积和重量方面表现出更佳疗效。
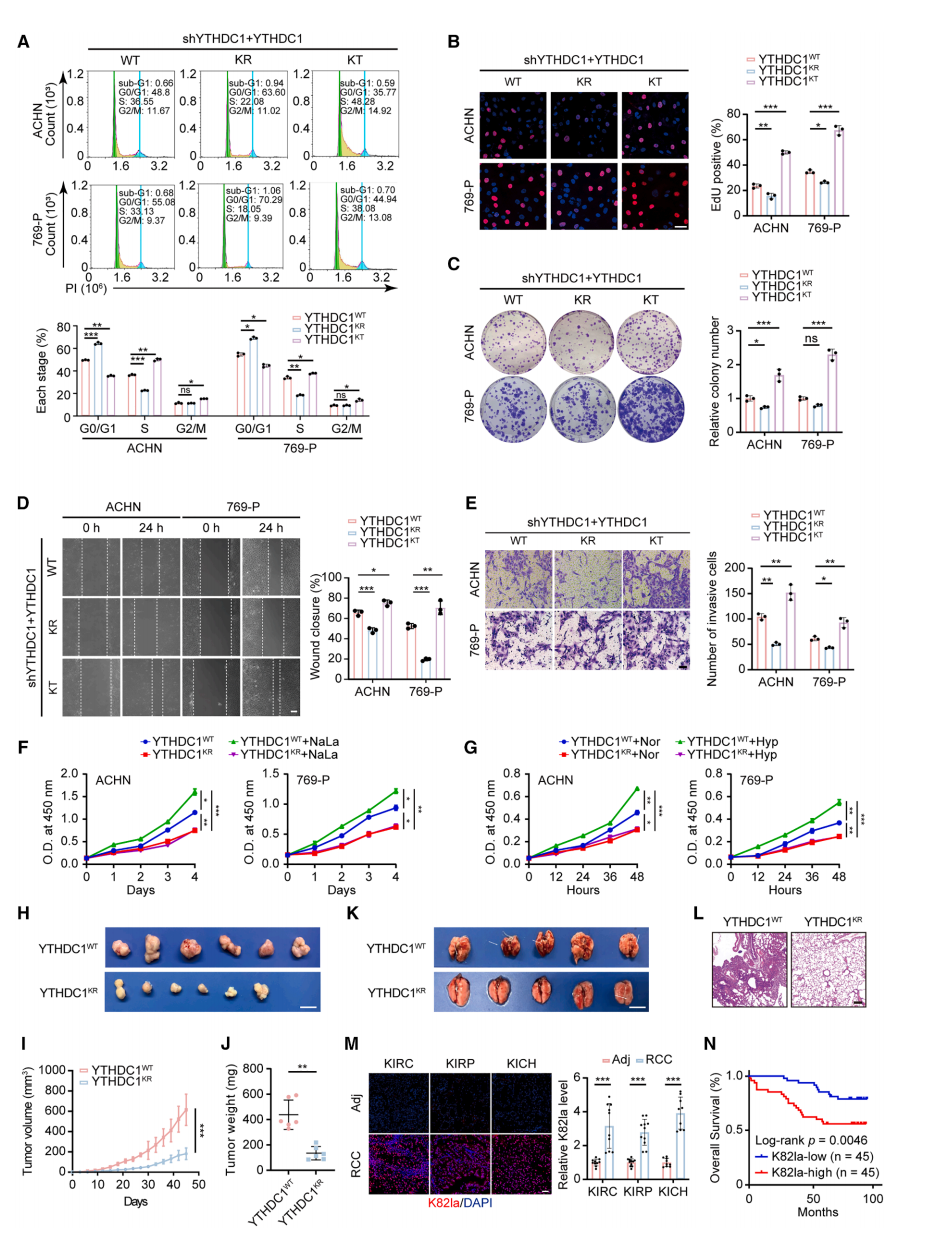
Figure 3. YTHDC1K82la promotes RCC malignancy
乳酸化修饰促使YTHDC1核内凝聚体增大
为探究YTHDC1K82la调控RCC恶性进展的机制,研究者分析了其蛋白结构。YTHDC1具有一个RNA识别YTH结构域和两个固有无序区,其中K82位点位于N端IDR内。受此启发,研究者推测乳酸化修饰可能偏好特定区域。结果显示,不同蛋白中46个(93%)差异乳酸化位点均位于IDR区域内,这提示缺氧诱导的乳酸化可能广泛调控IDR功能。
IDR可通过液相分离驱动凝聚体形成,进而影响染色质调控、基因表达和细胞命运。此外,通过免疫荧光检测内源性K82乳酸化YTHDC1时发现,在过表达p300的细胞中观察到离散点状结构而非弥散分布,表明p300介导的YTHDC1乳酸化可能调控其核内凝聚体。因此,研究者观察了YTHDC1乳酸化对细胞核内凝聚体的影响。与YTHDC1WT相比,YTHDC1KQ(另一种已报道的乳酸化模拟突变)和YTHDC1KT组的凝聚体明显增大、边缘更清晰,且光漂白后荧光恢复动力学检测显示其流动性减慢。缺氧诱导的乳酸化仅改变YTHDC1WT的凝聚状态,而对突变型无影响。同时,缺氧和乳酸钠处理并未影响YTHDC1的蛋白定位。通过乳酸钠和3-溴丙酮酸调控YTHDC1WT的乳酸化水平,发现乳酸钠组凝聚体增大且边缘清晰,而3-溴丙酮酸则破坏凝聚体结构,导致其尺寸显著减小。敲低p300后,缺氧处理无法再扩大细胞中凝聚体面积。综上所述,IDR区域的乳酸化修饰可能通过影响YTHDC1的相分离凝聚状态,进而调控RCC的恶性进展。
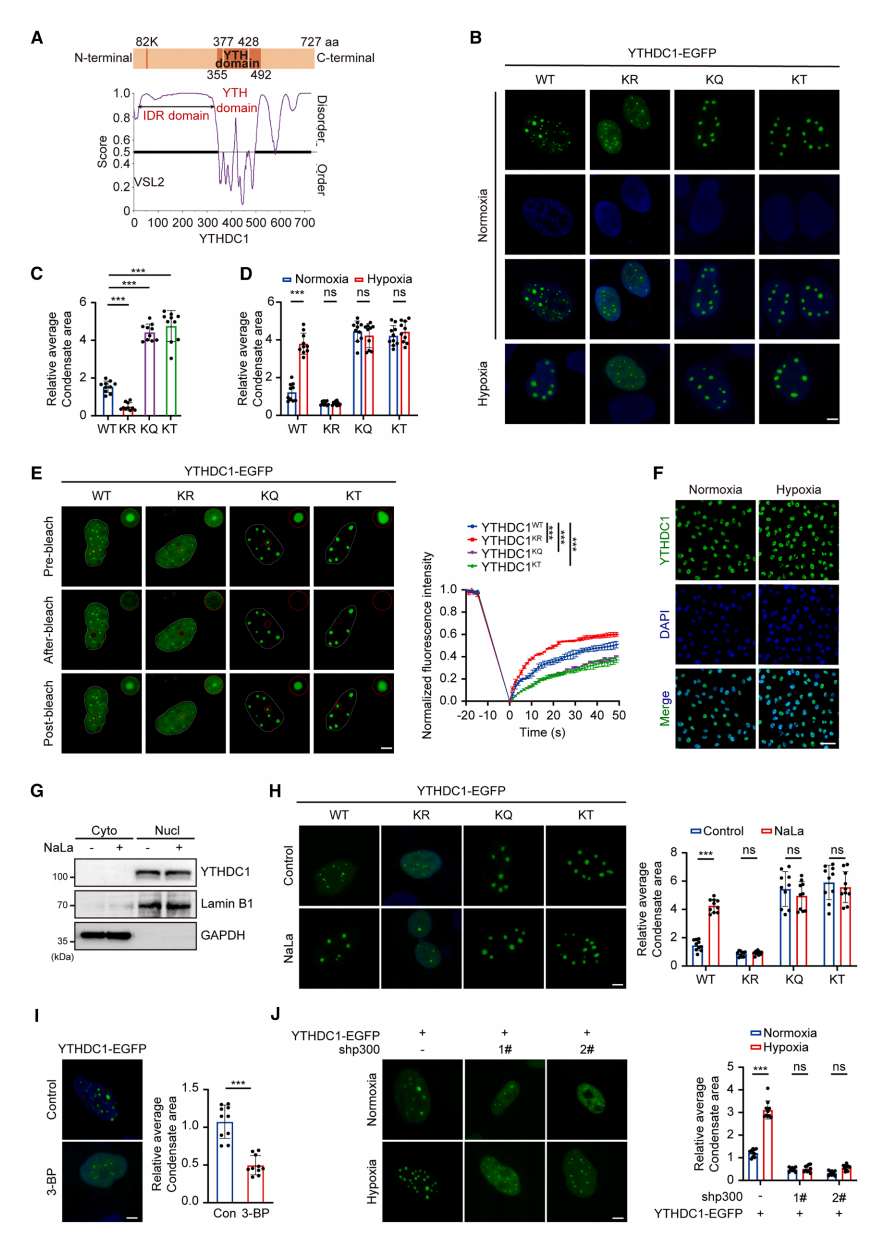
Figure 4. Lactylation enlarges YTHDC1 nuclear condensates
YTHDC1K82乳酸化修饰调控E2F2与BCL2 mRNA的表达
为探究YTHDC1WT/KT凝聚体影响RCC进展的分子基础,研究者对ACHN-YTHDC1WT/KT细胞进行RNA测序。结果显示存在大量表达差异基因,包括280个下调基因和319个上调基因。这些基因主要富集于p53信号通路、细胞周期等途径。其中上调基因(包括BCL2和E2F2)在细胞周期、p53信号通路中富集,而下调基因(包括BAX和TP53I3)则富集于p53信号通路、癌症转录失调等通路。随后在ACHN细胞中对基因表达变化进行验证,结果表明YTHDC1K82la可能调控细胞生长、迁移和凋亡相关基因的表达。
通过RNA免疫共沉淀测序技术(RIP-seq),研究者进一步鉴定YTHDC1靶向的mRNA。结果显示YTHDC1的m6A结合谱在编码区富集,主要识别基序为GGAC。RIP-seq共发现1,198个与YTHDC1结合的mRNA,与RNA-seq差异表达mRNA取交集后获得50个共同基因,其中前20个mRNA包含BCL2、E2F2等已知癌基因。RIP-RT-PCR、RIP实时荧光定量PCR及CLIP实时荧光定量PCR结果均证实E2F2和BCL2是YTHDC1的直接靶标。BCL2 mRNA(荧光原位杂交显示)与YTHDC1凝聚体(免疫荧光显示)在核内共定位,进一步表明YTHDC1凝聚体可与特定靶标mRNA结合。鉴于YTHDC1作为m6A阅读器的功能,甲基化RNA免疫共沉淀实验证实BCL2和E2F2转录本确实发生m6A修饰并与YTHDC1结合。
YTHDC1可通过调控染色质可及性调节转录活性。研究者检测发现YTHDC1K82乳酸化并未影响MYC、E2F2和BCL2的初始转录水平,提示其可能通过转录后机制调控靶基因表达。值得注意的是,YTHDC1K82la增强了其与BCL2、E2F2转录本的结合能力和共定位,但未改变这两个转录本的m6A修饰水平。这些结果表明YTHDC1K82la可能通过结合靶转录本来调控基因表达。此外,在高乳酸化YTHDC1细胞中,Bcl-2和E2F2的蛋白水平与其mRNA水平一致均呈现上调。
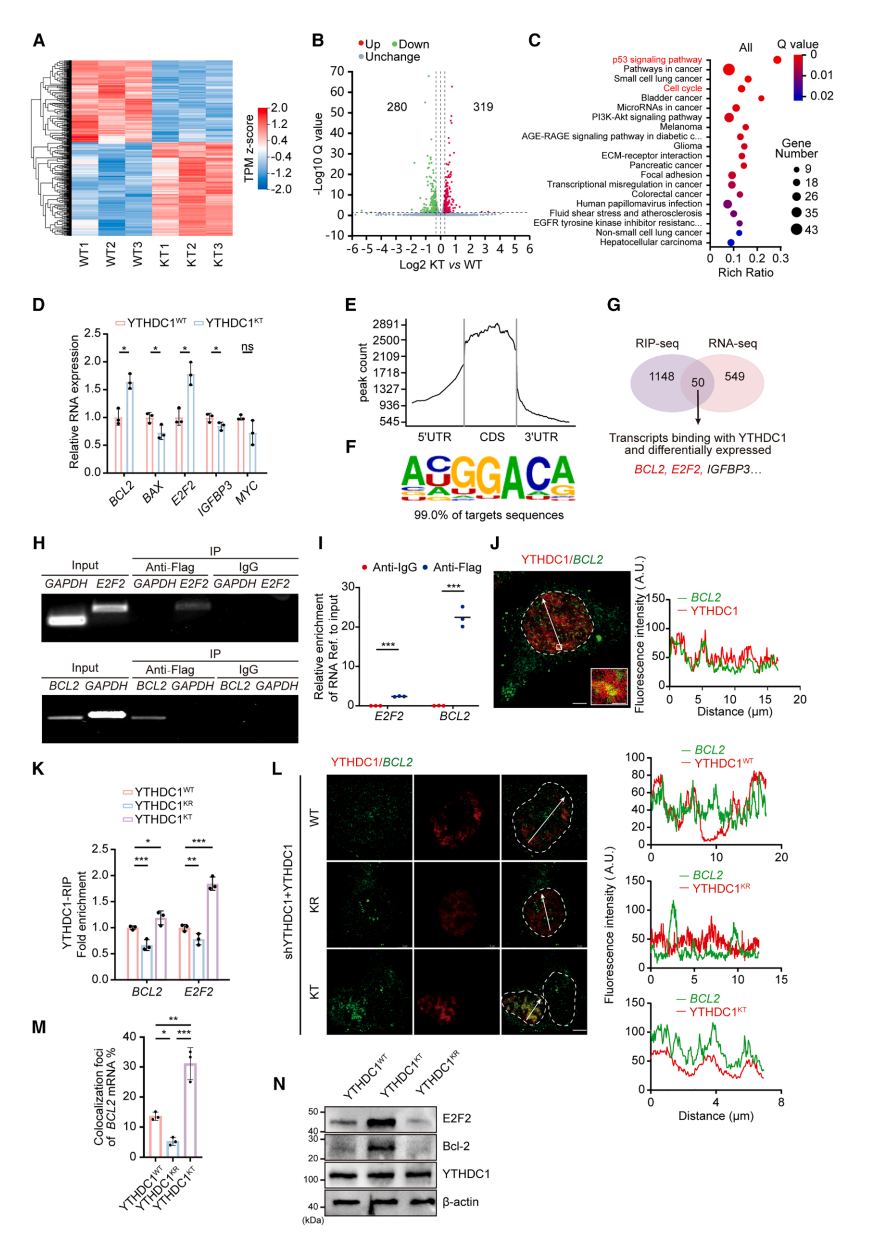
Figure 5. YTHDC1K82la regulates the expression of E2F2 and BCL2 mRNAs
YTHDC1K82乳酸化通过保护靶标mRNA免于降解促进肾癌进展
YTHDC1可调控转录后RNA加工过程,包括选择性剪接、RNA降解和核输出,从而影响RNA水平。该研究发现YTHDC1K82la能增强BCL2和E2F2转录本的稳定性。PolyA尾外泌体靶向复合物通过其核心组分PABPN1介导细胞核内mRNA降解。研究者通过荧光实验证实,YTHDC1KT组中mRNA与PABPN1的共定位减少,而YTHDC1KR组则呈现相反趋势。敲低PABPN1后,YTHDC1蛋白水平未受影响,但YTHDC1KT细胞中BCL2和E2F2的mRNA水平不再发生改变,而YTHDC1WT和YTHDC1KR组则出现升高。这些数据表明YTHDC1K82la可能通过增强相分离凝聚来保护BCL2和E2F2 mRNA免于降解。
YTHDC1同时也是促进mRNA核输出的关键因子。研究者观察到尽管YTHDC1KT细胞中BCL2 mRNA在核质区均增加,但其核质分布比例未发生改变,说明YTHDC1K82la并非通过调控mRNA出核来影响基因表达。
基于上述数据及Bcl-2和E2F2在肿瘤进展中的已知功能,研究者进一步探究了二者在YTHDC1K82la介导的RCC进展中的作用。结果显示,过表达E2F2可部分逆转YTHDC1KR细胞的细胞周期阻滞和恶性表型抑制,表明YTHDC1K82la的促瘤作用依赖于E2F2。此外,YTHDC1KR过表达细胞对舒尼替尼诱导的凋亡更敏感,而Bcl-2过表达能显著恢复其凋亡耐受,提示靶向YTHDC1K82la可能具有RCC临床治疗潜力。该研究最终揭示了靶向"YTHDC1K82la-相分离-BCL2/E2F2"轴在肾细胞癌治疗中的重要意义。
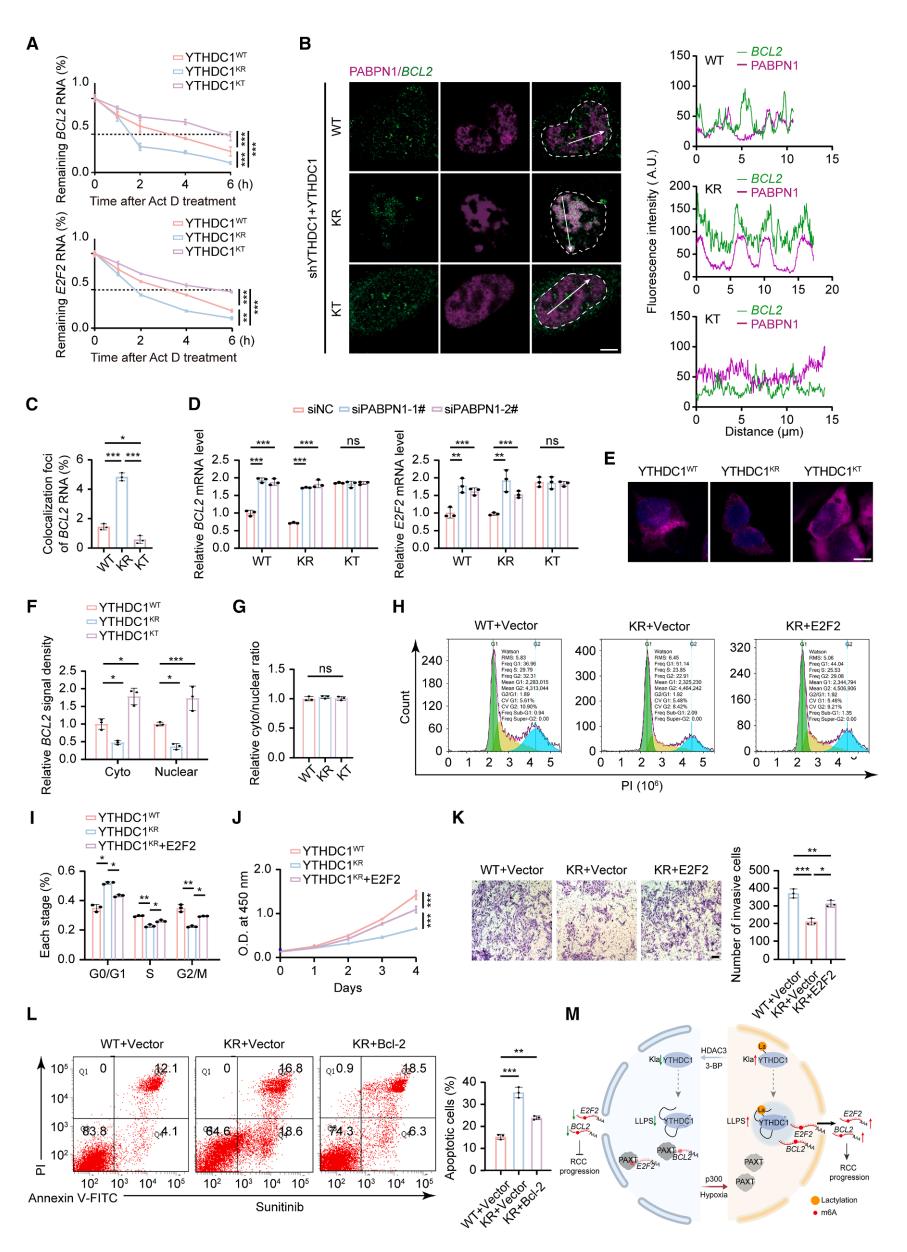
Figure 6. YTHDC1K82la promotes RCC progression via protecting target mRNAs from degradation
讨论:
该研究系统描绘了肾细胞癌中缺氧调控的乳酸化修饰全景图谱,并成功鉴定了缺氧条件下的关键乳酸化蛋白及位点(YTHDC1K82)。研究者提出一个潜在作用模型:YTHDC1K82la通过扩大相分离凝聚体来保护靶标mRNA(BCL2和E2F2)免于降解,从而促进RCC进展。通过阐释YTHDC1乳酸化调控相分离凝聚体及其RNA结合能力的分子机制,研究者为缺氧促进YTHDC1乳酸化驱动RCC进展的调控机制提供了新见解。抑制乳酸化修饰可能成为RCC的潜在治疗策略。
部分RCC以VHL突变为特征,该突变诱导的伪缺氧状态会影响组蛋白乳酸化水平并促进透明细胞肾癌进展。但值得注意的是,某些携带VHL突变的RCC细胞系中存在HIF1α基因缺失,这提示VHL突变-HIF1α上调可能并非RCC中乳酸化的唯一机制。该研究发现缺氧还可通过不依赖HIF的途径促进乳酸化,其具体机制仍有待深入探索。
固有无序区的翻译后修饰(如乙酰化、O-GlcNAc糖基化和磷酸化)可通过时空调控蛋白凝聚状态影响无膜细胞器形成。例如HP1γ第5位赖氨酸的去乙酰化会影响其核内凝聚并促进多发性骨髓瘤耐药,DDX3X的N端IDR乙酰化会损害液滴形成。该研究表明YTHDC1K82乳酸化可调控RCC细胞中该蛋白的核内凝聚。p300作为乳酸转移酶与YTHDC1相互作用并增强其凝聚,YTHDC1K82la通过相分离机制保护BCL2和E2F2免遭PAXT-外泌体复合物降解。研究者推测在缺氧应激下,核内YTHDC1快速感知代谢变化并发生乳酸化,形成相分离区室主动保护核内BCL2 mRNA免受PAXT介导的降解。不同mRNA是否通过特异的免降解机制受到保护,仍有待未来研究探索。特别值得注意的是,RNA结合蛋白的IDR可通过改变蛋白构象调控RNA结合,这一过程受翻译后修饰精细调控。该研究中IDR结构域内K82位点的乳酸化直接影响YTHDC1与RNA的结合能力,其深层机制值得进一步解析。总之,研究者的发现为揭示RNA结合蛋白如何连接乳酸化与相分离进而推动RCC进展提供了机制性见解。
另一项有趣发现是大多数差异乳酸化位点位于IDR区域,而乙酰化修饰更常见于具有规则二级结构的区域。这表明乳酸化与乙酰化对蛋白修饰区域具有不同偏好性。由于IDR在介导相分离和生物分子凝聚体形成中起关键作用,乳酸化位点在IDR的高比例分布提示该修饰可能更易影响液相分离过程。研究者的研究由此揭示了"乳酸化-IDR-相分离"之间潜在的内在关联。
综上所述,该研究阐明YTHDC1K82la通过诱导核内凝聚体扩张并隔离BCL2与E2F2转录本,从而保护其免于PAXT-外泌体复合物降解,展现了活细胞内精确的蛋白质时空调控机制。这些成果成功构建了"乳酸化修饰—RNA结合蛋白相分离凝聚—肾癌进展"的事件链条,为癌症治疗中靶向乳酸化与相分离的调控策略提供了理论基础与前瞻视角。
汇报人:吴婷婷
导师:任建君
审核:张宇阳、厚媛、任建君





